
对C、N、O元素的有关比较表述不正确的是 ( )
A. 氢化物稳定性:CH4<NH3<H2O
B. 第一电离能:C<N<O
C. 电负性:C<N<O
D. 氢化物沸点:CH4<NH3<H2O
科目:高中化学 来源:2015-2016学年新疆乌鲁木齐七十中高二下期末化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.CS2为V形的极性分子
B.Cl03- 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO32- 的中心原子均为sp3杂化,空间构型为正四面体结构
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高一下期末化学试卷(解析版) 题型:选择题
下列实验方案能达到实验目的的是
选项 | 实验方案 | 实验目的或结论 |
A | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中,溶液变黄色 | H2O2的氧化性比Fe3+强 |
B | 将一小块钠分别投入盛有水和乙醇的小烧杯中,钠与乙醇反应要平缓得多 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
C | 将某气体通入品红溶液,溶液褪色 | 气体中一定有SO2 |
D | 将铁棒和铜棒用导线连接后放入浓硝酸中,铜棒变细 | 铜的金属性强于铁 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下期末化学试卷(解析版) 题型:选择题
关于下列各实验装置的叙述中,正确的是 ( )
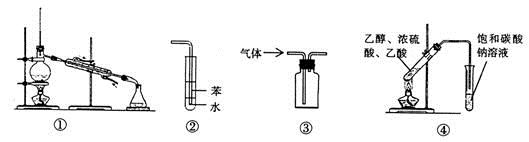
A. 装置①常用于分离互不相溶的液体
B. 装置②可用于吸收NH3
C. 装置③可用于收集NO、CO2等气体
D. 装置④可用于制备乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下期末化学试卷(解析版) 题型:选择题
下列实验相关叙述正确的是( )
A.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
B.实验室常采用铁屑、溴水、苯混合制溴苯
C.苯中含有少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去
D.一定物质的量浓度溶液的配置必须要用干燥的容量瓶,否则有误差
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二下期末化学试卷(解析版) 题型:填空题
铜及其化合物在工业上有许多用途。回答下列问题:
(1)某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:

①浸取反应中氧化剂的化学式为_______;滤渣Ⅰ的成分为MnO2、S和_________(写化学式)。
②“除铁”这一步反应在25℃进行,加入试剂A调节溶液PH为4后,溶液中铜离子最大浓度不超过__________mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
③“沉锰”(除Mn2+)过程中反应的离子方程式__________________________ 。
④ 滤液Ⅱ经蒸发结晶得到的盐主要是____________________ (写化学式)。
(2)某实验小组同学用电化学原理模拟湿法炼铜,进行了一系列探究活动。
①如下左图为某实验小组设计的原电池装置,盐桥内装载的是足量用饱和氯化钾溶液浸泡的琼脂,反应前,电极质量相等,一段时间后,两电极质量相差6.00 g,则导线中通过了________mol电子,若不考虑甲、乙两池电解质溶液中的离子向盐桥中移动,则甲、乙两池电解质溶液的总质量与实验开始前的电解质溶液的总 质量相差__________g
质量相差__________g

②其他条件不变,若将盐桥换成光亮的U形弯铜丝浸入甲池与乙池,如上右图所示,电流计指针偏转方向与先前一样,但偏转角度明显减小。一段时间后,乙池石墨棒浸入液面以下部分也析出了一层紫红色固体,则甲池铜丝附近溶液的pH________(填“减小”、“增大”或“不变”) ,乙池中石墨为________极(填“正”、“负”、“阴”或“阳”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二下期末化学试卷(解析版) 题型:选择题
绿原酸的结构简式如下图,则下列有关绿原酸的说法不正确的是( )

A.分子式为C16H18O9
B.既可以与氢气发生加成反应,又可以使酸性KMnO4溶液褪色
C.还能发生取代、加聚、消去等反应
D.在镍做催化剂的 情况下,1 mol绿原酸发生加成反应最多可消耗6 mol 氢气
情况下,1 mol绿原酸发生加成反应最多可消耗6 mol 氢气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽师大附中高一下期末化学试卷(解析版) 题型:选择题
某温度下,将Cl2通入NaOH溶液中,反应得到NaClO、NaClO3的混合液,经测定ClO-和ClO3-的浓度之比为1∶3,则Cl2与NaOH溶液反应时被还原的氯原子与被氧化的氯原子的物质的量之比( )
A. 21∶5 B.11∶3 C.3∶1 D.4∶1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下期末化学试卷(解析版) 题型:填空题
合理使用药物是保证身心健康、提高生活质量的有效手段。药物化学已经成为化学的一个重要领域。
(1)我国科学家屠呦呦因发现治疗疟疾的特效药——青蒿素,而获得2015年诺贝尔生理学或医学奖。青蒿素的结构简式如下图所示,其中的过氧基(—O—O—)具有强氧化性。请回答下列问题:

①青蒿素的分子式为 ;
②下列有关青蒿素的叙述中,正确的是 填字母).
A.青蒿素属于芳香族化合物
B.青蒿素具有强氧化性,可用于杀菌
C.青蒿素分子中的所有碳原子在同一个平面上
D.在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸) 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为:

请回答下列问题:
①制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是 (填字母).
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
②写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式 ;
③1mol乙酰水杨酸与足量的NaOH溶液反应,最多消耗NaOH物质的量为 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com