
下列物质的熔点高低顺序,正确的是
| A.金刚石>晶体硅>碳化硅 | B.K>Na |
| C.NaF<NaCl<NaBr | D.CI4>CBr4 |
D
解析A.原子晶体熔点,比较共价键键长,键长越短,键能越大,物质越稳定;键长:C-C<C-Si<Si-Si,熔点:金刚石>碳化硅>晶体硅;
B.金属晶体键能的大小比较看金属原子的半径大小 ,半径越小 键能越大,熔点越高。K<Na
C.离子晶体熔点,比较晶格能,离子半径越小,所带电荷越多,晶格能越大,离子晶体熔点越高;离子半径:F-<Cl-<Br-,熔点:NaF>NaCl>NaBr ;
D.分子晶体熔点,比较分子间作用力,相对分子质量越大,分子间作用力越大,熔点越高。
【考点定位】比较物质的熔点和沸点的高低,通常按下列步骤进行,首先比较物质的晶体类型,然后再根据同类晶体中晶体微粒间作用力大小,比较物质熔点和沸点的高低,具体比较如下:
一、判断所给物质的晶体类型,然后按晶体的熔点和沸点的高低进行比较,一般来说晶体的熔点和沸点的高低是:原子晶体>离子晶体>分子晶体,例如:晶体硅>氯化钠>干冰。但并不是所有这三种晶体的熔点和沸点都符合该规律,例如:氧化镁(离子晶体)>晶体硅(原子晶体)。而金属晶体的熔点和沸点变化太大,例如汞、铷、铯、钾等的熔点和沸点都很低,钨、铼、锇等的熔点和沸点却很高,所以不能和其它晶体进行简单的比较。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
| 代号 | 物质 | 结构式 | 水中溶解度/g (25℃) |
熔点/℃ | 沸点/℃ |
| A | 邻-硝基苯酚 |  |
0.2 | 45 | 100 |
| B | 对-硝基苯酚 | 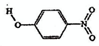 |
1.7 | 114 | 295 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省师大附中高二下学期期中考试化学试卷 题型:单选题
下列物质的熔点高低顺序,正确的是
| A.金刚石>晶体硅>碳化硅 | B.K>Na>Li |
| C.NaF<NaCl<NaBr | D.CI4>CBr4>CCl4>CH4 |
查看答案和解析>>
科目:高中化学 来源:2012届福建省高二下学期期中考试化学试卷 题型:选择题
下列物质的熔点高低顺序,正确的是
A、金刚石>晶体硅>碳化硅 B、K>Na>Li
C、NaF<NaCl<NaBr D、CI4>CBr4>CCl4>CH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com