
| A.分液、蒸馏 | B.蒸馏、分液 | C.分液、萃取 | D.萃取、分液 |
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源:不详 题型:填空题
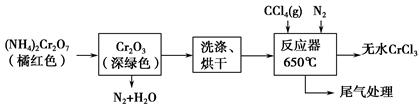
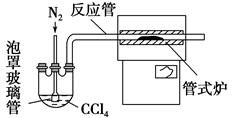
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
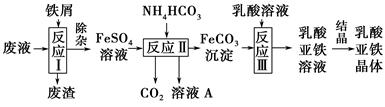
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
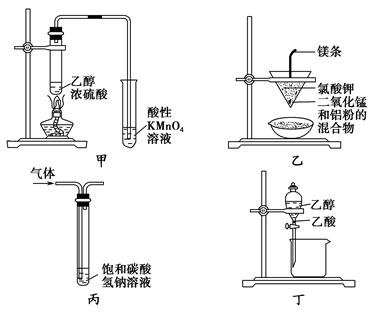
| A.甲图所示装置可以检验有乙烯生成 |
| B.乙图所示装置可以制取金属锰 |
| C.丙图所示装置用来洗气,除去CO2中的HCl气体 |
| D.丁图所示装置用来分离乙醇和乙酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
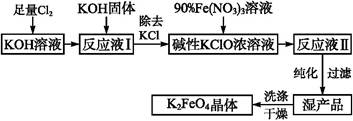
 KCl+KClO+H2O(条件:温度较低)
KCl+KClO+H2O(条件:温度较低) 5KCl+KClO3+3H2O(条件:温度较高)
5KCl+KClO3+3H2O(条件:温度较高) 2K2FeO4+6KNO3+3KCl+5H2O
2K2FeO4+6KNO3+3KCl+5H2O ;② 。
;② 。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化碳中混有SO2(饱和NaHCO3溶液) |
| B.氮气中混有氧气(灼热的铜网) |
| C.NaNO3溶液中混有Na2SO4〔Ba(NO3)2溶液〕 |
| D.氨气中混有水蒸气(浓硫酸) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.此法的优点之一是原料来源丰富 |
| B.该提取镁的过程中涉及置换、分解、复分解和氧化还原反应 |
| C.步骤①②③的目的是从海水中提取无水MgCl2 |
| D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+=Mg2++2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O| | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 33.7 | 11.1 | 6.34 |
 2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为 。
2KMnO4+2KOH+H2↑。与原方法相比,电解法的优势为 。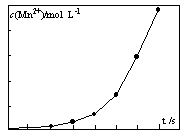
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 物质(括号内为杂质) | 试剂 | 方法 |
| A | Cl2(HCl ) | NaOH溶液 | 洗气 |
| B | Fe(Al) | NaOH溶液 | 过滤 |
| C | CO2(CO) | O2 | 点燃 |
| D | KNO3(KOH) | FeCl3溶液 | 过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com