
 �����ڼ��CO����Ӧԭ��Ϊ��
�����ڼ��CO����Ӧԭ��Ϊ��
 ����2L�ܱ������м�������
����2L�ܱ������м������� ����ͨ��1molCO��CO2���������
����ͨ��1molCO��CO2��������� ��ʱ��ı仯����ͼ��ʾ��
��ʱ��ı仯����ͼ��ʾ��
 _____________��
_____________�� ���������
��������� ���ɲ�ȡ�Ĵ�ʩΪ____________��
���ɲ�ȡ�Ĵ�ʩΪ____________�� Ϊ���������Խ�
Ϊ���������Խ� �Ļ������ֱ��ת��Ϊ���ᡣ
�Ļ������ֱ��ת��Ϊ���ᡣ ______________��
______________�� ________14(�>������<����=��)�����¶��´���ĵ��볣��K=__________(�ú�a��b��ʽ�ӱ�ʾ)��
________14(�>������<����=��)�����¶��´���ĵ��볣��K=__________(�ú�a��b��ʽ�ӱ�ʾ)�� ���Դ�������β���������÷�Ӧ���Ϊԭ��أ�������Na2O������ʣ��������缫��ӦʽΪ________________________________��
���Դ�������β���������÷�Ӧ���Ϊԭ��أ�������Na2O������ʣ��������缫��ӦʽΪ________________________________��

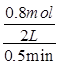 =0.8mol/(L��min)���ڱ����¶Ⱥ�������䣬����ʼ����CO(g)�����ʵ�����ԭ����2����������I2������Ϊԭ����2��������������������ԭ����2���������ʵ�����ԭ����2����ƽ��Ħ���������䣬�ܶ���ԭ����2����Ũ�������·�Ӧ��������ƽ���ʱ����٣���ab��ȷ���۷�Ӧ��a��ʱ��������������
=0.8mol/(L��min)���ڱ����¶Ⱥ�������䣬����ʼ����CO(g)�����ʵ�����ԭ����2����������I2������Ϊԭ����2��������������������ԭ����2���������ʵ�����ԭ����2����ƽ��Ħ���������䣬�ܶ���ԭ����2����Ũ�������·�Ӧ��������ƽ���ʱ����٣���ab��ȷ���۷�Ӧ��a��ʱ�������������� ���������
��������� ����ʹƽ��������Ӧ�����ƶ�����÷�ӦΪ���ȷ�Ӧ���ʿɽ����¶ȡ�
����ʹƽ��������Ӧ�����ƶ�����÷�ӦΪ���ȷ�Ӧ���ʿɽ����¶ȡ�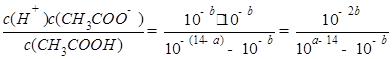 ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʳƷ���ڱ��������� |
| B��˫��ˮ������ʱ���������������� |
| C���Թ��н���þ��ˮ��Ӧʱ�������� |
| D�����۴���������ϡ���ᷴӦ��ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ʱ��(min) | 1 | 2 | 3 | 4 | 5 |
| �������(mL) | 50 | 120 | 232 | 290 | 310 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
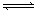 XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵����
XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵���� | A���٢ۢ� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
 CH3OH+H2O����ش��������⣺
CH3OH+H2O����ش��������⣺
|
|
|
|
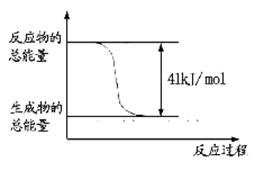
 д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ__ _��
д���ɶ�����̼�������Ʊ��״����Ȼ�ѧ����ʽ__ _��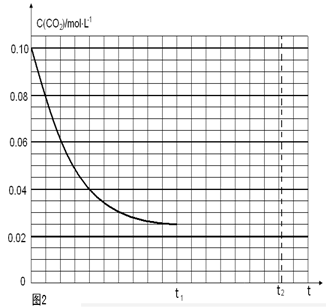
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

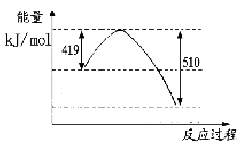
| A��ͼ�ٱ�ʾһ��������ij��ѧ��Ӧ��������ʱ��仯������ͼ���÷�Ӧһ��Ϊ���ȷ�Ӧ |
| B��ͼ�������߱�ʾ������������Һ�μӵ�������ҺŨ�ȵı仯����ͼ |
| C��ͼ�۱�ʾ������������ʵ���Ũ�ȵ�����ʹ��ᣬ�ֱ������þ�ۣ�����H2�����ʵ����ı仯 |
| D��ͼ��Ϊˮ�ĵ���ƽ������ͼ������A�㵽C�㣬�ɲ�����ˮ�м�������NaOH����ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)����H��0
2SO3(g)����H��0
| A�����˴������� | B����С������� | C�������¶� | D������SO3�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 AB��˵�������°�����������з�Ӧ��
AB��˵�������°�����������з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4NO(g)+ 6H2O(g)������������ȷ����
4NO(g)+ 6H2O(g)������������ȷ����| A���ﵽ��ѧƽ��ʱ��������������0 |
| B������λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬ |
| C���ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ�������� |
| D���ﵽ��ѧ��Ӧƽ��ı�������������������ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com