
对于密闭容器中可逆反应 A2(g)+3B2(g) 2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是
2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是
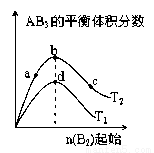
A. 加入催化剂可以使状态 d 变为状态 b
B. 若 T1>T2,则逆反应一定是放热反应
C. 达到平衡时 A2 的转化率大小为: b>a>c
D. 在T2 和n(A2)不变时达到平衡,AB3 的物质的量大小为: c>b>a
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:2016-2017学年山西省大同市高二2月月考化学试卷(解析版) 题型:选择题
对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是( )
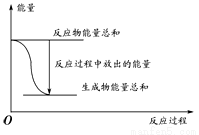
A. 反应过程中能量关系如上图表示,则该反应为放热反应
B. 若将该反应设计成原电池,锌为负极
C. 化学反应的焓变与反应方程式的计量数有关
D. 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列有关物质的浓度关系正确的是
A. 0.1mol•L-1HCl溶液与0.2mol•L-1氨水等体积混合(pH﹥7):c(NH4+)>c(Cl-)>c(NH3·H2O)>c(OH-)
B. Na2CO3溶液中:c(Na+)<c(CO32-)+c(HCO3-)
C. c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c(NH4Cl)>c((NH4)2SO4)
D. 0.1mol•L-1 (NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3·H2O)+c(Fe2+)=0.3mol•L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省凯里市高二下学期开学考试理综化学试卷(解析版) 题型:实验题
凯里一中2018届高一(1)班的两名同学用酸碱中和滴定的方法测定烧碱溶液的浓度。过程如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准硫酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且30秒内颜色不再改变为止,测得所耗硫酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL蒸馏水,测得所耗盐酸为V2mL。
试回答下列问题:
(1)滴定时边滴边摇动锥形瓶,眼睛应观察______________;
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)锥形瓶中的溶液从_______色变为_______色时,且30秒种不变化,停止滴定。
(3)该小组在步骤中①错误是______________,由此造成的测定结果分别是_______,(填偏高、偏低或无影响)。
(4)步骤②缺少的操作是______________________。
(5)如下图,是某次滴定时的滴定管中的液面,则其读数为_______mL。
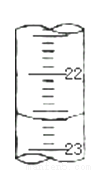
(6)根据下列数据
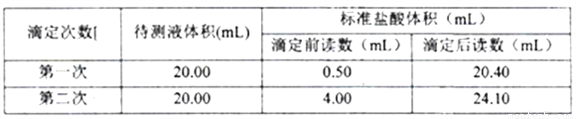
请计算待测烧碱溶液的浓度为______________mol/L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省凯里市高二下学期开学考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 22.4LO2中一定含有6.02×1023个氧原子
B. 将80gNaOH固体溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L
C. 18gH2O在标准状况下的体积是22.4L
D. 在标况下,20mLNH3与60mLO2所含的分子个数比为1:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二下学期开学考试化学试卷(解析版) 题型:选择题
下列各种叙述中正确的是
A. 在CH2=CH2分子中,存在4个σ键和一个π键
B. NH3、CO、CS2都是极性分子
C. N、O、F电负性大小:F>O>N;第一电离能大小:F>N>O
D. H2O的沸点比HF的沸点高,是由于水中氢键键能大
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期开学考试化学试卷(解析版) 题型:选择题
某同学将一块铝箔用砂纸仔细打磨,除去表面的保护膜,用坩埚钳夹住放在酒精灯火焰上加热,观察到的现象是( )
A. 剧烈燃烧 B. 发出耀眼白光 C. 熔化的铝滴落 D. 失去金属光泽
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省镇江市高二年级学业水平测试(必修)化学试卷(解析版) 题型:简答题
过氧化钙晶体(CaO2·8H2O)常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
(1)过氧化钙晶体可用下列方法制备:
CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl。
用如下制取装置制备过氧化钙晶体。

①装置A中发生反应的化学方程式为_______; 仪器X的名称为________。
②装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ.该反应是放热反应,温度低有利于提高CaO2·8H2O产率;
Ⅱ.________________________
③反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验晶体已洗涤干净的操作为__________________。
(2)测定产品中CaO2·8H2O含量的实验步骤如下:
步骤一:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入2mol·L—1的硫酸溶液,充分反应。
步骤二:向上述锥形瓶中加入几滴__________溶液。
步骤三:逐滴加入浓度为c mol·L—1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出三次平均消耗Na2S2O3溶液体枳为V mL。产品中CaO2·8H2O的质量分数为_________ (用字母表示)[已知:I2+2S2O32-=2I-+ S4O62-]
(3)钙在空气中燃烧生成氮化钙(Ca3N2),同时可能会生成CaO2。请限用下列试剂,设计实验检验钙在空气中燃烧所得固体中是否含有CaO2:______________(简要说明实验步骤、现象和结论)。限用试剂:稀盐酸、MnO2。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团第二师华山中学高二下学期学前考试化学试卷(解析版) 题型:选择题
一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
A. 4 mol NH3和5 mol O2反应,达到平衡时放出的热量为905.9 kJ
B. 平衡时v正(O2)=4/5v逆(NO)
C. 平衡后降低压强,混合气体的平均摩尔质量增大
D. 平衡后升高温度,混合气体中NO含量降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com