
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化.下列说法正确的是
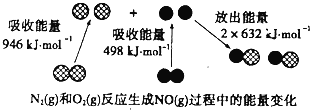
A. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
B. 通常情况下,N2(g)和O2混合能直接生成NO
C. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
D. 1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代以石油化工为基础的三大合成材料是⑴合成氨;⑵塑料;⑶医药;⑷合成橡胶;⑸合成尿素;⑹合成纤维;⑺合成洗涤剂。
A. ⑵⑷⑺ B. ⑵⑷⑹ C. ⑴⑶⑸ D. ⑷⑸⑹
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NaCl溶液的装置如图所示,下列说法不正确的是( )
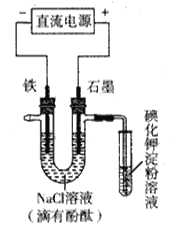
A. 铁电极上的电极反应式为Fe-2e-=Fe2+
B. 溶液中Na+由石墨电极向铁电极移动
C. 通电一段时间后,可看到铁电极附近溶液变红
D. 通电一段时间后,可看到试管中溶液变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸苯乙酯(![]() )是一种天然抗癌药物,在一定条件下能发生如下转化:
)是一种天然抗癌药物,在一定条件下能发生如下转化:
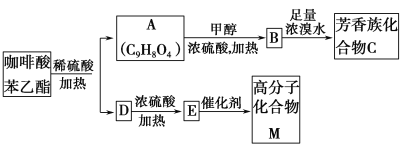
请填写下列空白:
(1)D分子中的官能团是________。
(2)高分子化合物M的结构简式是_____________________________________。
(3)写出A―→B反应的化学方程式:___________________________。
(4)B―→C发生的反应类型有____________________________。
(5)A的同分异构体很多种,其中同时符合下列条件的同分异构体有________种。
①苯环上只有2个取代基;②能发生银镜反应;
③能与碳酸氢钠溶液反应;④能与三氯化铁溶液发生显色反应。
(6)以下对A具有的性质描述正确的是________。
a.1 mol A最多消耗2 mol NaOH
b.一定条件下1 mol A最多能与1 mol氢气加成
c.能发生银镜反应
d.能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2(与Cl2的氧化性相近),常温下为气体,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放进行了研究。
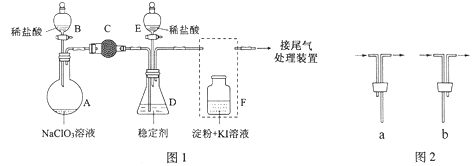
(1)安装F中导管时,应选用图2中的:___________。(填“a”或“b”)
(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式:____________________。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是:_________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________,该能层具有的原子轨道数为________。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H22NH3实现储氢和输氢。下列说法正确的是________。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH![]() 与PH
与PH![]() 、CH4、BH
、CH4、BH![]() 、ClO
、ClO![]() 互为等电子体
互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是__________________________。
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。
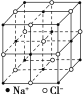
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则与Na+次近邻的Cl-个数为________,该Na+与跟它次近邻的Cl-之间的距离为________。
(2)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为________。(用含a、b的式子表示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com