
分析 (1)H++OH-═H2O,表示强酸或者强酸的酸式盐与可溶性强碱反应生成可溶性盐和水;
(2)硫酸铝为强电解质,完全电离;
(3)盐酸与碳酸氢钠反应生成氯化钠和水、二氧化碳;
(4)氢氧化钡与二氧化碳反应生成碳酸钡和水;
(5)碳酸根离子能够与钙离子反应生成碳酸钙,过量的碳酸钠与盐酸反应生成氯化钠和水、二氧化碳.
解答 解:(1)H++OH-═H2O,表示强酸或者强酸的酸式盐与可溶性强碱反应生成可溶性盐和水,可以表示氢氧化钡与盐酸反应,化学方程式:Ba(OH)2+2HCl=BaCl2+2H2O;
故答案为:Ba(OH)2+2HCl=BaCl2+2H2O;
(2)硫酸铝为强电解质,完全电离,电离方程式:Al2(SO4)3=2Al3++SO42-;
故答案为:Al2(SO4)3=2Al3++SO42-;
(3)盐酸与碳酸氢钠反应生成氯化钠和水、二氧化碳,离子方程式:HCO3-+H+═H2O+CO2↑;
故答案为:HCO3-+H+═H2O+CO2↑;
(4)氢氧化钡与二氧化碳反应生成碳酸钡和水,离子方程式:Ba2++2OH-+CO2═H2O+BaCO3↓;
故答案为:Ba2++2OH-+CO2═H2O+BaCO3↓;
(5)碳酸根离子能够与钙离子反应生成碳酸钙,过量的碳酸钠与盐酸反应生成氯化钠和水、二氧化碳,所以可以用碳酸钠溶液除去氯化钠溶液中的钙离子;
故答案为:碳酸钠溶液.
点评 本题考查了离子方程式的书写,电解质电离方程式的书写,化学方程式的书写,明确相关物质的性质是解题关键,注意除杂过程中不能引入新的杂质,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(H2)=0.1 mol•L-1•min-1 | B. | υ(N2)=0.2 mol•L-1•min-1 | ||
| C. | υ(NH3)=0.15 mol•L-1•min-1 | D. | υ(H2)=0.3 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
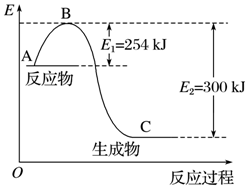 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
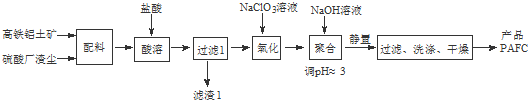
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com