
(共16分,没空2分)
已知下列热化学方程式:
①C(s)+H2O(s)===CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
②H2SO4(l)+NaOH(l)===Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
③C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+O2(g)===CO2(g) ΔH=-283 kJ·mol-1
⑤HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑥H2(g)+ O2(g)===H2O(1)
ΔH=-285.6kJ/mol
O2(g)===H2O(1)
ΔH=-285.6kJ/mol
⑦C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ΔH=-2220.0 kJ·mol-1
⑧ N2 (g)+ 3H2(g) === 2NH3 (g) ΔH=-92 kJ·mol-1
(1)上述热化学方程式中,不正确的有______________,不正确的理由分别是 _____________________________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式:______________________。
(3)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kJ,则混合气体中H2和C3H8的体积比是 。
(4)已知:H2O(1)=H2O(g);ΔH=+44.0kJ/mol写出丙烷燃烧生成CO2和气态水的热化学方程式
(5)上述反应中,表示燃烧热的热化学方程式有__________________________________;
表示中和热的热化学方程式有______________。
(6) 已知H—H键能为436 kJ/mol,H—N键能为391kJ/mol,则N≡N键的键能是_____________?
(1)①② ①中H2O的状态应为“g”;②中除H2O外其他物质的状态不是“l”应为“aq”
(2)C(s)+O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
(3)1:1 (4)C3H8(g)+5O2(g)===3CO2(g)+4H2O(g) △H=-2044kJ/mol
(5) ③④⑥⑦ ⑤ (6) 945.6kJ/mol
【解析】考查热化学方程式的判断、书写及反应热的计算等。
(1)①不正确,H2O的状态应为“g”;②不正确,除H2O外其他物质的状态不是“l”应为“aq”。
(2)根据盖斯定律可知,③-④即得到C(s)+O2(g)===CO(g),所以反应热是ΔH=-393.5 kJ·mol-1+283 kJ·mol-1=-110.5 kJ·mol-1。
(3)设混合气体中H2和C3H8的物质的量分别是x和y,则x+y=5mol。根据热化学方程式可知,
285.6kJ/mol×x+2220.0 kJ·mol-1×y=6262.5kJ,解得x=y=2.5mol,所以二者的体积之比是1:1。
(4)根据盖斯定律可得出生成气态水的热化学方程式是C3H8(g)+5O2(g)===3CO2(g)+4H2O(g) △H=-2044kJ/mol。
(5)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,因此表示燃烧热的是③④⑥⑦;中和热是在一定条件下,稀溶液中酸和碱反应生成1mol水时所放出的热量,因此答案选⑤。
(6)反应热是断键吸收的能量和形成化学键所放出的能量的差值,即436 kJ/mol×3+z-391kJ/mol×3×2=-92kJ/mol,解得z=945.6kJ/mol。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源:2012-2013学年广东省湛江二中高二第一次月考理科综合化学试卷(带解析) 题型:填空题
(共16分,没空2分)
已知下列热化学方程式:
①C(s)+H2O(s)===CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
②H2SO4(l)+NaOH(l)===Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
③C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+O2(g)===CO2(g) ΔH=-283 kJ·mol-1
⑤HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑥H2(g)+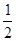 O2(g)===H2O(1) ΔH=-285.6kJ/mol
O2(g)===H2O(1) ΔH=-285.6kJ/mol
⑦C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ΔH=-2220.0 kJ·mol-1
⑧ N2 (g)+ 3H2(g)="==" 2NH3 (g) ΔH=-92 kJ·mol-1
(1)上述热化学方程式中,不正确的有______________,不正确的理由分别是 _____________________________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式:______________________。
(3)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kJ,则混合气体中H2和C3H8的体积比是 。
(4)已知:H2O(1)=H2O(g);ΔH=+44.0kJ/mol写出丙烷燃烧生成CO2和气态水的热化学方程式
(5)上述反应中,表示燃烧热的热化学方程式有__________________________________;
表示中和热的热化学方程式有______________。
(6) 已知H—H键能为436 kJ/mol,H—N键能为391kJ/mol,则N≡N键的键能是_____________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com