
【题目】将7g某Cu、Ag合金与一定量的浓硝酸反应,合金完全溶解后放出的气体与标准状况下0.56L氧气混合后,通入水中恰好完全被吸收,则合金中铜的质量为
A. 1.6g B. 2.4g C. 3.2g D. 4.8g
科目:高中化学 来源: 题型:
【题目】下列保存物质的方法正确的是( )
A. 新制氯水保存在棕色广口瓶中,并放在阴凉处
B. 波尔多液盛放在铁制容器中
C. 氨水易挥发,应密封且在低温处保存
D. 金属锂保存在煤油中,防止被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )(可能用到的相对原子质量:O—16 Na—23)
A. 含1 mol FeCl3的饱和溶液最多可形成胶体粒子数为NA
B. 1 mol Fe溶于过量硝酸,电子转移数为2 NA
C. 100 mL 2 mol·L-1碳酸钠溶液中,CO![]() 离子数为0.2 NA
离子数为0.2 NA
D. 7.8 g过氧化钠与水反应时转移的电子数为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室保存下列试剂,其中保存方法和理由描述都正确的是( )
编号 | 试剂 | 保存方法 | 理由 |
A | 钠 | 保存在煤油中 | 防止与空气中水、氧气接触发生反应 |
B | 液溴 | 密封保存在细口瓶中 | 防止升华 |
C | 浓硝酸 | 密封保存在铁器中 | 避免见光分解 |
D | 烧碱 | 存放在磨口玻璃塞的广口瓶中 | 防止与空气中氧气接触被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿酸是合成青蒿素的原料,可以由香草醛合成:
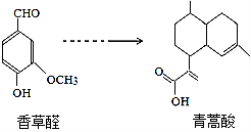
下列叙述正确的是( )
A.青蒿酸分子C15H14O2
B.在一定条件,香草醛可与HCHO发生缩聚反应
C.两种物质分别和H2反应,最多消耗H2 依次为4 mol和3 mol
D.可用FeCl3溶液或NaHCO3溶液鉴别化合物香草醛和青蒿酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件后发生下列反应能够导致固体物质增重的是( )
A. 铝与Fe2O3发生铝热反应 B. 将锌粒投入Cu(NO3)2溶液
C. 氢气通过灼热的CuO粉末 D. 二氧化碳通过Na2O2粉末
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组探究铜与浓硫酸的反应情况.甲.乙.丙三位同学进行了下列实验:取12.8g铜片和20ml.18mol/L的浓硫酸放在圆底烧瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余外,同时根据所学的知识认为还有较多的硫酸剩余.
(1)请写出铜跟浓硫酸反应的化学方程式: ,
试问:为什么较多的余酸不再与铜片继续反应?简述理由: .
可以证明有余酸的实验方案是 (填写字母,错选或多选扣分).
a.再加入铁粉 b.再滴入BaCl2溶液
c.再加入银 d.再滴入Na2CO3溶液
(2)甲学生设计求余酸浓度的实验方案是测定产生气体的量.其方法有多种,请问下列方案中不可行的是 (填写字母,错选或多选扣分).
a.将产生的气体缓缓通过预先称量盛有碱石灰的干燥管,结束反应后再次称量.
b.将产生的气体缓缓通入酸性高锰酸钾溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀.
c.用排水法测定其产生气体的体积(折算成标准状况).
d.用排饱和NaHSO3溶液的方法测出其产生气体的体积(折算成标准状况).
(3)乙同学设计测定余酸浓度的实验方案是:测定反应后的混合液中Cu2+的量.在反应后的溶液中加蒸馏水稀释至100ml,加入足量Na2S溶液,充分反应后,过滤.洗涤.干燥、称量沉淀.请写出生成沉淀的离子方程式: .
(4)根据甲、乙两同学的实验方案,除测算产生气体的物质的量或反应掉的铜的物质的量外,尚缺少的测量数据是 .
(5)丙同学提出甲、乙两同学的实验方案设计的复杂,为此他设计了下列较为简易的实验方案:取出反应后的铜片,进行洗涤.干燥.称量.若称得剩余铜片的质量为Wg,测得反应后溶液的体积为Vml,请计算剩余硫酸的物质的量浓度= mol/L(用含W.V的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com