
(14分)根据下图所示的转化关系填空(假设每一步反应的反应物均恰好反应完)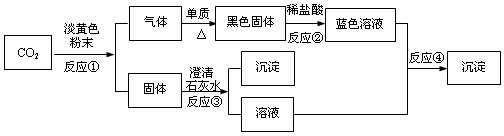
(1)写出反应①的化学方程式: 。
此反应中,氧化剂与还原剂的个数比为 。当有3.2 g气体产生时,消耗淡黄色固体的物质的量是_______mol,固体增重_______g;
(2)写出反应②、③、④的离子方程式:
②
③
④
(1)2Na2O2+2CO2=2Na2CO3+O2; 1︰1; 0.2, 5.6;
(2)CuO+2H+=Cu2++H2O Ca2++CO32-=CaCO3↓ Cu2++2OH-=Cu(OH)2↓
解析试题分析:能和CO2反应的淡黄色粉末应该是过氧化钠。过氧化钠和CO2反应生成氧气和碳酸钠。碳酸钠和澄清的石灰水反应生成碳酸钙白色沉淀和氢氧化钠。根据反应②生成的是蓝色溶液可知,该溶液中含有铜离子,所以单质是铜,黑色固体是氧化铜。氧化铜和盐酸反应生成氯化铜,氯化铜和氢氧化钠反应生成蓝色沉淀氢氧化铜。
考点:考查过氧化钠的性质、铜及其化合物的转化
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,难度不大,学生不难得分。解框图题的关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。


科目:高中化学 来源: 题型:
已知![]() -氨基酸在一定条件下能与亚硝酸(HNO2)反应得到
-氨基酸在一定条件下能与亚硝酸(HNO2)反应得到![]() -羟基酸。
-羟基酸。
如![]() ,试根据下图所示的转化关系回答有
,试根据下图所示的转化关系回答有
关的问题(产物中生成的H2O等小分子均省略):
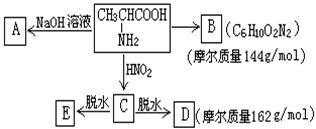
(1)写出下列物质的结构简式:A 、
|