
分析 (1)醋酸是弱酸,不能完全电离;
(2)在醋酸钠溶液中,醋酸钠根离子水解导致溶液显示碱性;
(3)a.弱酸、弱碱、水属于弱电解质,强酸强碱,大部分盐等属于强电解质;
b.酸和碱均能抑制水的电离;
c.若两溶液混合后pH<7,则溶液中醋酸的电离程度大于醋酸根离子的水解.
解答 解:(1)醋酸是弱酸,不能完全电离,0.10mol/L的CH3COOH溶液中氢离子浓度小于0.10mol/L,则其溶液的pH>1;
强氧化钠为强碱,0.10mol/L的溶液中氢氧根离子浓度为0.10mol/L,溶液的pH=13,
故答案为:>;,1;
(2)两溶液等体积混合后所得溶液为醋酸钠溶液,在醋酸钠溶液中,醋酸钠根离子水解导致溶液显示碱性,涉及的离子反应为:、CH3OO-+H2O?CH3COOH+OH-,
故答案为:CH3COOH+OH-=CH3OO-+H2O;CH3OO-+H2O?CH3COOH+OH-;
(3)a.醋酸属于弱电解质,氢氧化钠属于强电解质,故a错误;
b.酸和碱均能抑制水的电离,故b正确;
c.若两溶液混合后pH<7,则溶液混合后醋酸剩余,醋酸的电离程度大于醋酸根离子的水解程度,溶液中离子浓度存在关系:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故c正确;
故答案为:bc.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,涉及弱电解质的电离、盐的水解、溶液酸碱性与溶液pH的计算以及溶液中离子浓度的大小关系比较等知识,明确溶液酸碱性与溶液pH的关系及计算方法为解答关键.


科目:高中化学 来源: 题型:多选题
| A. | 16g | B. | 8g | C. | 40g | D. | 0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、乙炔、溴苯分子中的所有原子均是共平面 | |
| B. | 乙烷(CH3CH3)和异丁烷( )互为同系物 )互为同系物 | |
| C. | 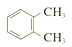 和 和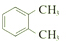 互为同分异构体 互为同分异构体 | |
| D. | 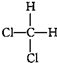 与 与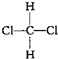 是同一种物质 是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、Cl-、SO42- | B. | Ba2+、Na+、SO42-、Cl- | ||
| C. | NH4+、I-、K+、OH- | D. | Cu2+、Na+、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、纤维、油脂、淀粉、聚乙烯都是高分子化合物 | |
| B. | 蛋白质的水解产物为氨基酸 | |
| C. | 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 | |
| D. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
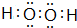 .F的原子结构示意图为:
.F的原子结构示意图为: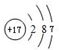 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com