
 �״�����Ҫ�Ļ���ԭ�ϣ��ڻ����������й㷺��Ӧ�ã�
�״�����Ҫ�Ļ���ԭ�ϣ��ڻ����������й㷺��Ӧ�ã�| t/min | 0 | 1 | 3 | 5 |
| n��H2��/mol | 8 | 5 | 4 | 4 |
���� ��1������Ŀ��Ϣ����֪�״��������ɼ����������������������ٷֽ�õ��״���CO����ƽ��д����ʽ��
��2�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ����Ӧ��Ҳ������Ӧ�����㣻
��3���ٸ���v=$\frac{��c}{��t}$����v��H2��������������֮�ȵ����仯ѧ������֮�ȼ���v��CH3OH����
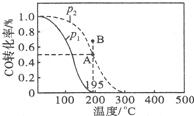
��ͼ��֪�����¶����ߣ�CO��ת���ʽ��ͣ�˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ���
����ͼ��֪����ͬ�¶��£�ѹǿP2ƽ��ʱCO��ת���ʸ�������ӦΪ���������С�ķ�Ӧ�����ѹǿ��ƽ���ƶ���Ӱ���жϣ�
����20L���ܱ������У������ʵ���֮��1��2����CO��H2����ʼ������Ũ��Ϊ$\frac{8mol}{20L}$=0.4mol/L��COŨ��Ϊ$\frac{4mol}{20L}$=0.2mol/L���ɱ������ݿ�֪��3min����ƽ�⣬ƽ��ʱ����Ũ��Ϊ$\frac{4mol}{20L}$=0.2mol/L����
CO��g��+2H2��g��?CH3OH��g��
��ʼ��mol/L����0.2 0.4 0
ת����mol/L����0.1 0.2 0.1
ƽ�⣨mol/L����0.1 0.2 0.1
����ƽ�ⳣ������ʽK=$\frac{c��C{H}_{3}OH��}{c��CO����{c}^{2}��{H}_{2}��}$���㣮
��� �⣺��1������Ŀ��Ϣ����֪�״��������ɼ����������������������ٷֽ�õ��״���CO����Ӧ����ʽΪ��2CH3OH��HCOOCH3+2H2����HCOOCH3��CH3OH+CO����
�ʴ�Ϊ��2CH3OH��HCOOCH3+2H2����HCOOCH3��CH3OH+CO����
��2����֪����2H2O��1��=2H2��g��+O2��g����H=+571.5kJ•mol-1
��3H2��g��+CO2��g��=CH3OH��1��+H2O��1����H=-137.8kJ•mol-1
���ݸ�˹���ɣ��١�$\frac{3}{2}$+�ڵã�2H2O��1��+CO2��g��=CH3OH��l��+$\frac{3}{2}$O2��g�����ʡ�H=$\frac{3}{2}$����+571.5kJ•mol-1��+��-137.8kJ•mol-1��=+719.45kJ•mol-1��
�ʴ�Ϊ��+719.45��
��3�����ɱ������ݿ�֪��3min�ڲμӷ�Ӧ����Ϊ8mol-4mol=4mol����v��H2��=$\frac{\frac{4mol}{20L}}{3min}$=$\frac{1}{15}$mol/��L��min��������֮�ȵ����仯ѧ������֮�ȣ���v��CH3OH��=$\frac{1}{2}$v��H2��=$\frac{1}{2}$��$\frac{1}{15}$mol/��L��min��=0.033mol/��L��min����
��ͼ��֪�����¶����ߣ�CO��ת���ʽ��ͣ�˵�������¶ȣ�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ����Q��0��
�ʴ�Ϊ��0.033mol/��L��min��������
����ͼ��֪����ͬ�¶��£�ѹǿP2ƽ��ʱCO��ת���ʸ�������ӦΪ���������С�ķ�Ӧ������ѹǿƽ��������Ӧ�����ƶ���CO��ת������ߣ���ѹǿP1��P2��
�ʴ�Ϊ��P1��P2����ͬ�¶��£�ѹǿP2ƽ��ʱCO��ת���ʸ�������ӦΪ���������С�ķ�Ӧ������ѹǿƽ��������Ӧ�����ƶ���CO��ת������ߣ�
����20L���ܱ������У������ʵ���֮��1��2����CO��H2����ʼ������Ũ��Ϊ$\frac{8mol}{20L}$=0.4mol/L��COŨ��Ϊ$\frac{4mol}{20L}$=0.2mol/L���ɱ������ݿ�֪��3min����ƽ�⣬ƽ��ʱ����Ũ��Ϊ$\frac{4mol}{20L}$=0.2mol/L����
CO��g��+2H2��g��?CH3OH��g��
��ʼ��mol/L����0.2 0.4 0
ת����mol/L����0.1 0.2 0.1
ƽ�⣨mol/L����0.1 0.2 0.1
��ƽ�ⳣ��K=$\frac{0.1}{0.1��0��{2}^{2}}$=25��
�ʴ�Ϊ��25��
���� ��������ƴ������Ŀ���漰��Ӧ�ȼ��㡢��ѧƽ��ͼ��Ӧ���ʼ��㡢��ѧƽ��Ӱ�����ء�ƽ�ⳣ������ȣ����ؿ���ѧ����������������������������ʽ�ڻ�ѧƽ������Ӧ�ã�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ds��Ԫ�� | B�� | ����Ԫ�� | C�� | ����Ԫ�� | D�� | s��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
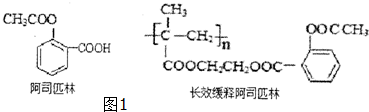
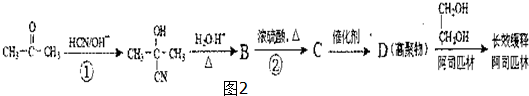
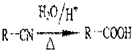 ���ش����⣺
���ش����⣺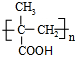 ��
��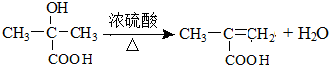 ��
��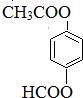 ��ֻдһ�֣���
��ֻдһ�֣����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ϳɰ���Ӧ�ڵ������ܹ��Է����У�����Ϊ��Ӧ�����֮�ʹ������������֮�� | |
| B�� | Ԫ�ط����ǿ���ȷ���������Ƿ���C��H��O��N��S��Cl��Br��Ԫ�أ�ԭ�����չ�����ȷ�������к�����Щ����Ԫ�� | |
| C�� | ��������Ԫ���������ڹ���Ԫ����Ѱ�Ҹ������������Ĵ������Խ��ͻ�ѧ��Ӧ�Ļ�ܣ��Ӷ��ܺõĽ���Ч�� | |
| D�� | ���߷ֱ���ӫ�������ܹ��۲쵽���׳߶ȵ����ʣ��������Ի�õ�������Һ�еķ���ͼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| CO2ת���� T���棩 | 10min | 20min | 30min | 40min |
| T1 | 30% | 65% | 75% | 75% |
| T | 45% | 50% | a1 | a2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
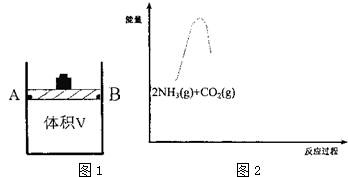
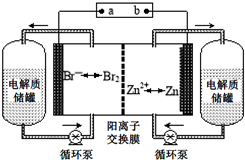 п��Һ�������һ�����͵绯ѧ����װ�ã���ͼ��ʾ�������ҺΪ�廯пˮ��Һ���������Һ�ڵ���ʴ��͵�ؼ䲻��ѭ��������˵������ȷ���ǣ�������
п��Һ�������һ�����͵绯ѧ����װ�ã���ͼ��ʾ�������ҺΪ�廯пˮ��Һ���������Һ�ڵ���ʴ��͵�ؼ䲻��ѭ��������˵������ȷ���ǣ�������| A�� | �ŵ�ʱ������ʴ����е�������Ũ������ | |
| B�� | ���ʱ�缫a���ӵ�Դ�ĸ��� | |
| C�� | �ŵ�ʱ�����ĵ缫��ӦʽΪZn-2e-�TZn2+ | |
| D�� | �����ӽ���Ĥ����ֹBr2��Znֱ�ӷ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ����ʵ������ | ʵ���Լ� | �¶ȼ�λ�� |
| A | ��ȡ��ϩ | Բ����ƿ������ƿ�������ܡ��ƾ��� | Ũ���ᡢ�Ҵ� | ��ӦҺ�� |
| B | �ᴿ�Ҵ� | ������ƿ�������ܡ���ƿ���нӹ� | 75%���Ҵ� | ֧���ܿ� |
| C | �к��Ȳⶨ | �ձ������β�������� | �������ơ����� | �ᡢ���ӦҺ�� |
| D | ������ | �ձ����Թܡ��ƾ��� | ������Һ�������� | ˮԡ���ձ�ˮ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com