
【题目】Ⅰ.人们每天都要摄入大量的淀粉类物质,以维持机体的营养均衡。这是因为淀粉[化学式为(C6H10O5)n]在淀粉酶作用下或在酸性环境下可以水解成葡萄糖[化学式是C6H12O6],请回答下列问题:
(1)淀粉的摩尔质量为______________;
(2)将90 g葡萄糖溶于水,配成1 L溶液,所得溶液溶质的物质的量浓度为________;
(3)把淀粉溶于沸水中,制成淀粉溶液,回答下列问题。
①如何通过实验证明淀粉溶液是胶体:______________(填现象名称)。
②在淀粉溶液中加入少量氯化钠晶体,并装入半透膜袋,系紧袋口,把它悬挂在盛有蒸镏水的烧杯里充分反应。能从半透膜里析出的分散质的化学式是____________,该操作的名称是____________。
Ⅱ.食品安全关系着国民生计,影响食品安全的因素很多。
(1)丁苯橡胶的结构简式如图所示: ,它是由________(写结构简式)发生加聚反应生成的。
,它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH=CH—CH2—CH=CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是________。
A.分子式为C18H34O2 B.一定条件下能与甘油(丙三醇)发生酯化反应
C.能和NaOH溶液反应 D.能使酸性KMnO4溶液褪色
【答案】162n g/mol 0.5mol/L 丁达尔现象 NaCl 渗析 ![]() 和CH2=CHCH=CH2 BCD
和CH2=CHCH=CH2 BCD
【解析】
Ⅰ.(1)淀粉是由n个C6H10O5链节构成的,故摩尔质量为162n g/mol;
(2)90g葡萄糖的物质的量为![]() =0.5mol,溶液体积为1L,所以浓度为0.5mol/L;
=0.5mol,溶液体积为1L,所以浓度为0.5mol/L;
(3)①胶体的特有的性质是丁达尔效应,故可以用丁达尔效应来证明淀粉溶液是胶体;
②胶体不能透过半透膜,淀粉不能透过半透膜,溶液可以透过,故析出的物质是NaCl,此操作为渗析;
Ⅱ.(1)该高聚物链节上只有碳原子,一般为加聚产物,链节中有双键,所以双键左右各两个碳原子共4个碳原子为一组,剩余两个碳原子为一组,断开得到单体为![]() 和CH2=CHCH=CH2;
和CH2=CHCH=CH2;
(2)A.根据该物质的结构简式可知其分子式为C18H32O2,故A错误;
B.亚油酸含有羧基,可以与甘油发生酯化反应,故B正确;
C.亚油酸含有羧基,可以与NaOH溶液反应,故C正确;
D.亚油酸含有碳碳双键,可以被酸性高锰酸钾溶液氧化使其褪色,故D正确;
综上所述选BCD。


科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液滴加到己二酸![]() 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是

A.曲线M表示pH与 的变化关系
的变化关系
B.![]() 的数量级为
的数量级为![]()
C.NaHX溶液中![]()
D.当混合溶液呈中性时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() ,在容积为2L的密闭容器中进行。起始时无
,在容积为2L的密闭容器中进行。起始时无![]() ,且
,且![]() 和
和![]() 物质的量相等,在 不同条件下进行反应,气体总浓度随时间的变化如图所示。下列说法 不正确的是
物质的量相等,在 不同条件下进行反应,气体总浓度随时间的变化如图所示。下列说法 不正确的是
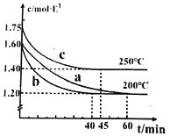
A.反应b从开始到![]() 的平均反应速率为
的平均反应速率为![]()
B.b可能是加入了催化剂
C.反应c从开始到![]() 的转化率为
的转化率为![]()
D.对比a,c曲线能说明,在同一时刻,该反应的反应速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 对此聚合物分析正确的是( )
对此聚合物分析正确的是( )
A. 其单体是CH2=CH2和HCOOC2H5
B. 它是缩聚反应产物
C. 其单体是CH2=CH-COOC2H5
D. 其链节是CH3CH2-COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏联科学家欧巴林教授在其著作中曾说:“生命起源于甲烷”,英国科学家巴纳尔教授则认为生命是从二氧化碳和水开始的。与之相关的转化关系如图所示(部分反应条件已略去):

(1)A的结构式为________;C中官能团的电子式为________;反应②的反应类型为________。
(2)写出下列物质的结构简式:D________;H________。
(3)C→D的化学方程式为__________;二氧化碳和水经光合作用生成葡萄糖的化学方程式为_________。
(4)在自然界中纤维素与水可在甲烷菌的催化作用下生成甲烷和二氧化碳,写出该反应的化学方程式并配平:
_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键、氢键和范德华力的叙述中,不正确的是( )
A.金属键是金属离子与“电子气”之间的强烈作用,金属键无方向性和饱和性
B.共价键是原子之间通过共用电子对形成的化学键,共价键有方向性和饱和性
C.范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大
D.氢键不是化学键而是一种较弱的作用力,所以氢键只存在于分子与分子之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a升CO2气体通过足量Na2O2所得的气体与b升NO相混和时,可得到c升气体(相同状况),以下表达式中错误的是( )
A. 若a<b,则c>0.5(a+b) B. 若a>b,则c=0.5(a+b)
C. 若a=b,则c=0.5(a+b) D. 若a<b,则c<0.5(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将agFe2O3和Al2O3的样品溶解在过量的200mL物质的量浓度为0.05mol/L的H2SO4溶液中,然后向其中加入NaOH溶液使Al3+、Fe3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
A.0.1mol/LB.0.2mol/LC.0.4mol/LD.0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是_____________________。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液C.浓氨水 D.酸性KMnO4溶液
②乙同学取560 mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为_______。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。
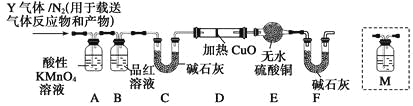
(3)装置B中试剂的作用是_______________________。
(4)分析Y气体中的Q2气体是如何生成的_____________(用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加洗气瓶M于_______(填序号)。
A.A之前 B.A—B间
C.B—C间 D.C—D间
(6)如果气体Y中含有Q1,预计实验现象应是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com