
 在一条鱼、虾绝迹的小河边有四座工厂甲、乙、丙、丁(如图),它们排出的废液里,每个工厂只有Na2CO3、CuCl2、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:(1)甲处河水呈乳白色;(2)乙处河水呈浅蓝色浑浊;(3)丙处河水由浑变清;(4)丁处产生气泡,河水仍清.请推断:
在一条鱼、虾绝迹的小河边有四座工厂甲、乙、丙、丁(如图),它们排出的废液里,每个工厂只有Na2CO3、CuCl2、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:(1)甲处河水呈乳白色;(2)乙处河水呈浅蓝色浑浊;(3)丙处河水由浑变清;(4)丁处产生气泡,河水仍清.请推断:

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
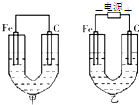 如图所示,甲、乙两池的电极材料都是铁棒与碳棒,请回答:
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为
(1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为查看答案和解析>>
科目:高中化学 来源: 题型:
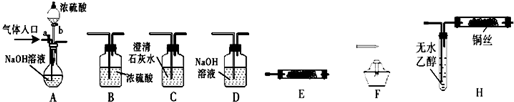
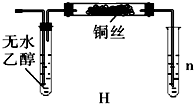
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可加入硫酸以提高电解质的导电性 |
| B、充电时LiFePO4只发生还原反应 |
| C、充电过程中,电池正极材料的质量增大 |
| D、放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
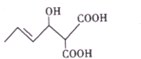
| A、其分子式为C7H10O5 |
| B、分子中含有三种官能团 |
| C、1mol该物质能与3mol NaOH溶液反应 |
| D、能使溴的四氯化碳溶液或酸性高猛酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向煮熟的豆浆中加入石膏或卤水以生产豆腐 |
| B、工厂用高压电极除粉尘 |
| C、氢氧化铁胶体中加入足量稀硫酸形成黄色溶液 |
| D、午后林间透过缕缕阳光 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com