
| A、利用盐酸刻蚀石英制作艺术品 |
| B、在常温下可用铝制容器贮藏运输稀硫酸 |
| C、纯碱可作治疗胃酸过多的一种药剂 |
| D、在金属与非金属的分界处,可以找到半导体材料 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、水的分解反应是放热反应 |
| B、氢气是二级能源 |
| C、使用氢气作燃料有助于控制温室效应 |
| D、在这一反应中,光能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年.元素周期表体现了元素位构性的关系,揭示了元素间的内在联系.如图是元素周期表的一部分,回答下列问题.
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年.元素周期表体现了元素位构性的关系,揭示了元素间的内在联系.如图是元素周期表的一部分,回答下列问题.| 实验步骤 | 实验现象与结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程中的能量关系可用如图简单表示(图中的△H表示生成1mol产物的数据).
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程中的能量关系可用如图简单表示(图中的△H表示生成1mol产物的数据).查看答案和解析>>
科目:高中化学 来源: 题型:
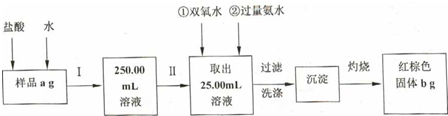
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正反应方向移动 |
| B、a<c+d |
| C、D的体积分数增大 |
| D、A的转化率变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
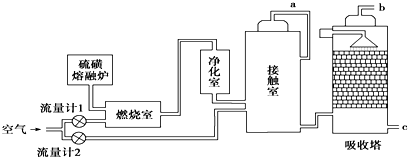
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com