
【题目】下列说法正确的是
A.植物油氢化产物属于烃类
B.制作集成电路板的酚醛树脂可导电
C.石油经催化裂化与裂解可获得较多的气态烯烃等产品
D.鸡蛋清中滴加1%醋酸铅溶液产生的沉淀能重新溶于水
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】[2015江苏][双选]在体积均为1.0 L的两恒容密闭容器中加入足量的相同的炭粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

A.反应CO2(g)+C(s)![]() 2CO(g)的ΔS>0、ΔH<0
2CO(g)的ΔS>0、ΔH<0
B.体系的总压强p总:p总(状态Ⅱ)>2p总(状态Ⅰ)
C.体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D.逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁钾矾[KxFey(SO4)m·nH2O]常用作工业媒染剂。其组成可用如下方法测定:
①准确称取2.0120g样品配成100mL溶液A。
②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.466g。
③准确量取25.00mL溶液A,加入足量的KI溶液,以淀粉为指示剂,用0.1250 mol·L-1的Na2S2O3溶液滴定,消耗8.00mL至终点(已知:I2+2Na2S2O3=2NaI+Na2S4O6)。
(1)要检验出A溶液中存在的Fe3+,可以加入 溶液。
(2)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-5 molL-1,应保持溶液中c(Ba2+)≥ mol·L-1。
(3)步骤③中判断滴定终点的方法是 。
(4)通过计算确定铁钾矾的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水资源开发利用的部分过程如图所示:

下列说法不正确的是
A. 海水淡化的常用方法有蒸馏法、 电渗析法和离子交换法
B. 可通过分液的方法分离溴单质和苯的混合物
C. 提纯时,所加试剂可依次为 BaCl2、 NaOH、 Na2CO3、盐酸
D. 精盐、 NH3和 CO2是侯德榜制碱工业的主要原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若甲烷与氯气以物质的量之比1:3混合,在光照下得到的有机产物:(1)CH3Cl,(2)CH2Cl2,(3)CHCl3,(4)CCl4,其中正确的是( )
A.只有(1)B.只有(3)C.只有(1)(2)(3)D.(1)(2)(3)(4)都有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以空气和镁为原料制备 Mg3N2 的装置如图所示(夹持和加热装置略去):
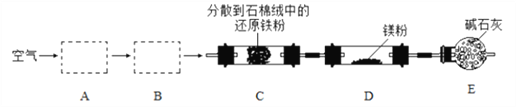
下列说法正确的是
A. 装置 A、B 中可依次加入浓硫酸、NaOH 溶液
B. 装置 E 中碱石灰的作用是吸收尾气
C. 实验时, 应先加热 C,通入一段时间空气后再加热D
D. 若去掉装置 C,对产品纯度无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔是物质的量的单位,简称摩,符号为mol
C. 摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D. 氢氧化钠的摩尔质量是40
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界能源消费的90%以上依靠化学技术。
(1)工业制氢的一个重要反应是利用CO还原H2O(g)。
已知:C(石墨,s)+O2(g)═CO2(g) △H=-394k J/mol
2C(石墨,s)+O2(g)═2CO(g) △H=-222k J/mol
H2(g)+1/2O2(g)═H2O(g) △H=-242k J/mol
则CO还原H2O(g)的热化学方程式为_________________________。
(2)氢能被视为最具发展潜力的绿色能源,写出碱式氢氧燃料电池的工作时的负极电极反应:_______。
(3)一种新型锂离子二次电池——磷酸铁锂(LiFePO4)电池。作为正极材料的磷酸铁锂在充、放电时的局部放大示意图如下图,写出该电池充电时的阳极电极反应__________。

(4)LiOH是制备锂离子电池正极材料的重要原料,其电解法制备装置如上图。气体a通入淀粉KI溶液中,发现溶液变蓝,持续一段时间后,蓝色逐渐褪去。则M极为电源的________(填“正”或“负”)极,B极区电解液为_______溶液(填化学式),该离子交换膜是________(填“阳”或“阴”)离子交换膜。
(5)上图所示装置(阴、阳极均为惰性电极)可用于电解尿素(CONH2)2)的碱性溶液制取氢气。该装置中阳极的电极反应式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com