
| A. | 常温下pH=13的溶液中:NH4+、Na+、Cl-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ | |
| C. | 能够与金属Cu常温下反应放出气体的溶液:Na+、Al3+、SO42-、K+ | |
| D. | 漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
分析 A.pH=13的溶液中存在大量氢氧根离子,铵根离子与氢氧根离子反应;
B.能与铝反应的溶液呈酸性或强碱性,铵根离子与氢氧根离子反应,硝酸根离子在酸性条件下与铝反应不会生成氢气;
C.能够与金属Cu常温下反应放出气体的溶液具有强氧化性,四种离子之间不反应,都不易被氧化;
D.漂白粉具有强氧化性,能够氧化亚铁离子.
解答 解:A.常温下pH=13的溶液呈碱性,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,在溶液中不能大量共存,故A错误;
B.能与金属铝反应放出氢气的溶液中存在大量氢离子或氢氧根离子,NO3-在酸性条件下与铝反应不会生成氢气,NH4+与氢氧根离子反应,在溶液中不会大量共存,故B错误;
C.能够与金属Cu常温下反应放出气体的溶液具有强氧化性,Na+、Al3+、SO42-、K+之间不发生反应,都不易被氧化,在溶液中能够大量共存,故C正确;
D.漂白粉的水溶液具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的NaCl溶液是指由1mol NaCl和1000mL水配制成的溶液 | |
| B. | 从1L 0.5mol•L-1的NaCl溶液中取出100mL,剩余溶液物质的量浓度为0.45mol•L-1 | |
| C. | 标准状况下,18克H2O所含的氧原子数目为NA | |
| D. | 0℃时,2mol Cl2的体积不可能为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
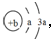 ,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题:
,Y、Z为同周期金属元素,其中Y为短周期元素中原子半径最大的元素,Z为地壳中含量最高的金属元素,W的最高价氧化物对应水化物可以与其气态氢化物反应生成盐G,盐G溶液呈酸性,回答下列问题: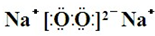 ,所含有的化学键类型为离子键和共价键.
,所含有的化学键类型为离子键和共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+ NO3- I-SO42- | B. | MnO4- K+NO3-Na+ | ||
| C. | K+Al3+Cl-SO42- | D. | Mg2+SO32-Br-Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 食品添加剂种类很多,其中的一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐 | |
| C. | 抗酸药的种类很多,如碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等 | |
| D. | 某些蔬菜和水果在人体代谢后,生成碱性物质,所以称为碱性食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的沸点:Z>M | |
| C. | X、Z与M不可能存在同一离子化合物中 | |
| D. | Y2Z的溶液:c(Y+):c(Z2-)>2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和热的测定实验时,眼睛要注视温度计的刻度变化 | |
| B. | 萃取时,将混合物充分振荡后,需静置,待液体分层明显后才能分液 | |
| C. | 中和滴定实验时,为了使滴定终点的现象更加明显,可以滴加较多的指示剂 | |
| D. | 蒸馏时,温度计的读数刚达到某物质的沸点,不能立即收集馏出物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com