
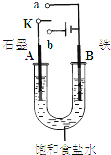
某课外活动小组同学用右图装置进行相关的实验,试回答下列问题。

(1)若开始时开关K与a连接,则A极的电极反应式为 。
(2)若开始时开关K与b连接,则总反应的离子方程式为 。在该实验中,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后(设NaCl足量)加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则有0.2 mol电子转移
(3)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。
A.C(s) + H2O(g) =" CO(g)" + H2(g) △H > 0
B.NaOH(aq) + HC1(aq) =" NaC1(aq)" + H2O(1) △H < 0
C.2H2(g) + O2(g) = 2H2O(1) △H<0
(4)电解原理在化学工业中有着广泛的应用。右图中,a为电解液,X和Y是两块电极板,回答下列问题:

(4)①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为 。通过一段时间后,向所得溶液中加入8g CuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为 。
(17分)
(1)2H2O + O2↑+4e-=4OH- (3分)
(2)2Cl- + 2H2O 电解 2OH- + H2↑ + Cl2↑(3分) ②④(2分)
(3)C(2分)
(4)①2CuSO4+2H2O 电解 Cu+O2↑+2H2SO4(3分) 0.2mol(2分)
②Cu -2e- = Cu2+ (2分)
【解析】
试题分析:(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,故答案为:Fe-2e-=Fe2+;
(2)开关K与b连接,装置为电解池,铁为阴极,发生还原反应,氢离子得到电子生成氢气,电解饱和食盐水生成氢氧化钠、氢气和氯气,电解过程中阳离子向阴极移动,①错误,A生成氯气,能使湿润KI淀粉试纸变蓝,②错误,反应一段时间后加适量HCl气体可恢复到电解前电解质的浓度,③错误,若标准状况下B极产生2.24L氢气,转移0.2mol电子,④正确,故答案为:2H++2e-=H2↑; 2Cl-+2H2O 2OH-+H2↑+Cl2↑;②正确。
2OH-+H2↑+Cl2↑;②正确。
(3)放热反应中,△H<0,形成原电池的反应必须为氧化还原反应,故选C。
(4)①电解CuSO4溶液,生成Cu单质、O2和H2SO4,方程式为2CuSO4+2H2O 电解 Cu+O2↑+2H2SO4。8g CuO,即0.1mol,根据质量守恒定律,反应的CuSO4为0.1mol,故电解过程中转移的电子的物质的量为0.2mol。
②阳极上失电子,故Y极的电极反应式为Cu -2e- = Cu2+。
考点:原电池和电解池的工作原理 原电池的设计 电极反应式的书写
点评:本题考查原电池和电解池原理和原电池的设计,解题时要注意分析电极反应及生成物,能设计成原电池的反应必须是放热反应,同时必须是氧化还原反应。


科目:高中化学 来源: 题型:
 某课外活动小组同学用如图装置进行实验,试回答下列问题.
某课外活动小组同学用如图装置进行实验,试回答下列问题.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2008?东莞模拟)某课外活动小组同学用右图装置进行实验,试回答下列问题.
(2008?东莞模拟)某课外活动小组同学用右图装置进行实验,试回答下列问题.
| ||
| ||
 气、氧气、硫酸和氢氧化钾.
气、氧气、硫酸和氢氧化钾.查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组同学用如图装置进行实验,试回答下列问题:
某课外活动小组同学用如图装置进行实验,试回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组同学用右图装置进行实验,试回答下列问题.
某课外活动小组同学用右图装置进行实验,试回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com