

分析 (1)NH4Al(SO4)2水解显酸性,NH4HSO4主要是因为电离出H+显酸性;
(2)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
②根据电荷守恒定律解题;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.C点溶液呈碱性.
解答 解:(1)NH4Al(SO4)2水解显酸性,NH4HSO4主要是因为完全电离出的H+显酸性,故pH相同的NH4Al(SO4)2的浓度须远大于大于NH4HSO4溶液的浓度,则NH4Al(SO4)2中c(NH4+) 大于NH4HSO4中c(NH4+),故答案为:>;
(2)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为I,故答案为:I;
②根据电荷守恒,可以求出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol•L-1[c(OH-)太小,可忽略],故答案为:10-3;
(3)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4,(NH4)2SO4的水解对水的电离有促进作用;而b、c、d三点溶液均含有NH3•H2O,而NH3•H2O抑制水的电离,故a点溶液中水的电离程度最大;
c点溶液呈碱性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)>c(H+),故答案为:a;c(Na+)>c(SO42-)>c(NH4+)>c(OH-)>c(H+).
点评 本题考查盐类的水解和离子浓度大小的比较,题目难度较大,(2)②为易错点,注意根据守恒思想解题.


科目:高中化学 来源: 题型:选择题
| A. | 硝酸铵自发地溶于水 | |
| B. | H2O(l)═H2O(g)△H=+44.0kJ•mol-1 | |
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量NaOH固体时动作缓慢 | B. | 定容时俯视刻度线 | ||
| C. | 定容后振荡发现液面低于刻度线 | D. | 未洗涤烧杯和玻璃棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 化学反应中能量变化的大小与反应物的质量密切相关 | |
| C. | 中和反应的反应热可以通过实验测得 | |
| D. | 实验法是获取反应热数据的唯一方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 常温常压下,22.4L CO2和SO2混合气体含有2NA个O原子 | |
| C. | 22.4 L CH4与18 g H2O所含有质子数均为10NA | |
| D. | 常温常压下,80g SO3含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丙烷(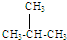 )也叫异丁烷 )也叫异丁烷 | |
| B. | 蛋白质和糖类均为天然高分子化合物 | |
| C. | 乙烯和丙烯只能发生加成反应,不能发生取代反应 | |
| D. | 苯使溴水褪色的原因是发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com