
| 1∶4解析:方法一:设H2SO4、CuSO4、Fe的物质的量为x、y、z.
Fe+H2SO4====FeSO4+H2↑ 1mol 1mol x x Fe+CuSO4====FeSO4+Cu 1mol 1mol 1mol y y y 由题意得:Fe粉加入前质量=生成铜的质量+剩余铁粉的质量. 即56g/mol×z=64g/mol×y+56g/mol×(z-x-y) 解得:y=7x 所以有 方法二:设H2SO4、CuSO4的物质的量分别为x、y. Fe + H2SO4====FeSO4+H2↑ 1mol 1mol x x Fe + CuSO4====FeSO4+Cu 1mol 1mol 1mol y y y 由题意知:减少的质量与增加的质量相等 56x+56y=64y 所以有y=7x
|


科目:高中化学 来源: 题型:013
把足量的铁粉投入硫酸和硫酸铜的混合液中,充分反应后,所得的金属粉末的质量和原来加入的铁粉质量相等.则原溶液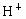 与
与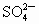 的物质的量之比为
的物质的量之比为
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:021
把足量的铁粉投入硫酸和硫酸铜的混合液中,充分反应后,剩余金属粉末的质量与原来加入的铁粉质量相等,则原溶液中
[ ]
A.1∶4 B.2∶7 C.1∶2 D.3∶8
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
把足量的铁粉投入硫酸和硫酸铜的混合溶液中,充分反应后,所得金属粉末的质量与原来加入的铁粉的质量相等,则原溶液中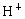 与
与 的物质的量之比为
的物质的量之比为
[ ]
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
把足量的铁粉投入硫酸和硫酸铜的混合液中,充分反应后,所得的金属粉末的质量和原来加入的铁粉质量相等.则原溶液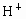 与
与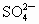 的物质的量之比为
的物质的量之比为
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com