
 2HIЃЈgЃЉЃЌЁїHЃМ0ЁЃЗДгІДяЕНЦНКтКѓЃЌИФБфЯТСаЬѕМўЃЌФмЪЙЗДгІЫйТЪБфТ§ЕФЪЧЃЈN2ВЛВЮМгЗДгІЃЉ
2HIЃЈgЃЉЃЌЁїHЃМ0ЁЃЗДгІДяЕНЦНКтКѓЃЌИФБфЯТСаЬѕМўЃЌФмЪЙЗДгІЫйТЪБфТ§ЕФЪЧЃЈN2ВЛВЮМгЗДгІЃЉ| AЃЎБЃГжШнЦїШнЛ§ВЛБфЃЌЯђЦфжаМгШы1mol H2 |
| BЃЎБЃГжШнЦїШнЛ§ВЛБфЃЌЯђЦфжаМгШы1mol N2 |
| CЃЎБЃГжШнЦїФкбЙЧПВЛБфЃЌЯђЦфжаМгШы1mol N2 |
| DЃЎБЃГжШнЦїФкбЙЧПВЛБфЃЌЯђЦфжадйМгШы1mol H2КЭ1mol I2 |

| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
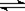 xC(g)+2D(g)ЃЌЕБЗДгІДяЕНЦНКтЪБЃЌЩњГЩ0.4 mol DЃЌВЂВтЕУCЕФЦНКтХЈЖШЮЊ0.4 mol/LЃЌЯТСаа№ЪіжаВЛе§ШЗЕФЪЧ
xC(g)+2D(g)ЃЌЕБЗДгІДяЕНЦНКтЪБЃЌЩњГЩ0.4 mol DЃЌВЂВтЕУCЕФЦНКтХЈЖШЮЊ0.4 mol/LЃЌЯТСаа№ЪіжаВЛе§ШЗЕФЪЧ| AЃЎxЕФжЕЮЊ2 | BЃЎAЕФзЊЛЏТЪЮЊ40% |
| CЃЎBЕФЦНКтХЈЖШЮЊ0.8 mol/L | DЃЎDЕФЬхЛ§ЗжЪ§ЮЊ20% |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎКЯГЩАБЕФЗДгІЮТЖШПижЦдк500ЁцНјааЁЁ |
| BЃЎгУФбШмFeSЙЬЬхГ§ШЅЙЄвЕЗЯЫЎжаЕФPb2+ |
| CЃЎДђПЊЬМЫсвћСЯЛсгаДѓСПЦјХнУАГі |
| DЃЎЪЕбщЪвгУХХБЅКЭЪГбЮЫЎЕФЗНЗЈЪеМЏТШЦј |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
 CO2ЃЋH2ЃЌДяЕНЦНКтЪБЩњГЩ0.7molЕФCO2ЃЌШєЦфЫћЬѕМўКЭCOЕФЦ№ЪМСПВЛБфЃЌвЛПЊЪМОЭМгШы4mol H2O(g)ЃЌдђДяЕНЦНКтЪБЩњГЩЕФCO2ПЩФмЪЧ
CO2ЃЋH2ЃЌДяЕНЦНКтЪБЩњГЩ0.7molЕФCO2ЃЌШєЦфЫћЬѕМўКЭCOЕФЦ№ЪМСПВЛБфЃЌвЛПЊЪМОЭМгШы4mol H2O(g)ЃЌдђДяЕНЦНКтЪБЩњГЩЕФCO2ПЩФмЪЧ| AЃЎ0.6mol | BЃЎ0.95mol | CЃЎ1mol | DЃЎ1.5mol |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎДђПЊЦћЫЎЦПЪБЃЌгаДѓСПЦјХнвчГі |
| BЃЎдкХфжЦСђЫсбЧЬњШмвКЪБЭљЭљвЊМгШывЛЖЈСПЬњЗл |
| CЃЎАБЫЎгІУмБеБЃДцЗХжУгкЕЭЮТДІ |
| DЃЎЪЕбщЪвгУХХБЅКЭЪГбЮЫЎЕФЗНЗЈЪеМЏТШЦј |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
 ЁЂYЁЂZБэЪОдЊЫиЗћКХЃЉЁЃЬжТлЩЯЪіЪЕбщЙ§ГЬжаРызгХЈЖШЕФДѓаЁЫГађЁЂЖдгІШмжЪЕФЛЏбЇЪНКЭШмвКЕФpHЁЃЪдЬюаДБэжаПеАзЃЈвЊЧѓЬюаДгаЙиСЃзгЛЏбЇЪНЃЉЃК
ЁЂYЁЂZБэЪОдЊЫиЗћКХЃЉЁЃЬжТлЩЯЪіЪЕбщЙ§ГЬжаРызгХЈЖШЕФДѓаЁЫГађЁЂЖдгІШмжЪЕФЛЏбЇЪНКЭШмвКЕФpHЁЃЪдЬюаДБэжаПеАзЃЈвЊЧѓЬюаДгаЙиСЃзгЛЏбЇЪНЃЉЃК| | РызгХЈЖШгЩДѓЕНаЁЕФЫГађ | ШмжЪЕФЛЏбЇЪН | ШмвКЕФpH |
| I | c(XY+4)>c(ZЁЊ)>c(OHЁЊ)>c(H+) | | pH>7 |
| II | c(XY+4)=c(ZЁЊ) | XY4ZЁЂXY3ЁЄH2O | |
| III | | XY4Z | pH<7 |
| IV | c(ZЁЊ)>c(H+)>c(XY+4)> >c(OHЁЊ) | | pH<7 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
 Z(g)+2W(g) ЁїHЃМ0ЁЃДяЕНЦНКтЃЈЂёЃЉЪБЃЌBжаУмЖШБфЮЊдРДЕФ
Z(g)+2W(g) ЁїHЃМ0ЁЃДяЕНЦНКтЃЈЂёЃЉЪБЃЌBжаУмЖШБфЮЊдРДЕФ ЃЌЪдЛиД№ЃК
ЃЌЪдЛиД№ЃК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
 ЃЌH2(g)ЃЋCO2(g)
ЃЌH2(g)ЃЋCO2(g) H2O(g)ЃЋCO(g)ЕФЦНКтГЃЪ§KЃН
H2O(g)ЃЋCO(g)ЕФЦНКтГЃЪ§KЃН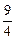 ЁЃИУЮТЖШЯТдкМзЁЂввЁЂБћШ§ИіКуШнУмБеШнЦїжаЃЌЭЖШыH2(g)КЭCO2(g)ЃЌЦфЦ№ЪМХЈЖШШчЯТБэЫљЪОЃК
ЁЃИУЮТЖШЯТдкМзЁЂввЁЂБћШ§ИіКуШнУмБеШнЦїжаЃЌЭЖШыH2(g)КЭCO2(g)ЃЌЦфЦ№ЪМХЈЖШШчЯТБэЫљЪОЃК| Ц№ЪМХЈЖШ | Мз | вв | Бћ |
| c(H2)/ molЁЄLЁЊ1 | 0.010 | 0.02 0 0 | 0.020 |
| c(CO2)/ molЁЄLЁЊ1 | 0.010 | 0.010 | 0.020 |
| AЃЎЦНКтЪБЃЌввжаCO2ЕФзЊЛЏТЪДѓгк60% |
| BЃЎЦНКтЪБЃЌМзКЭБћжаH2ЕФзЊЛЏТЪОљЪЧ60% |
| CЃЎЦНКтЪБЃЌБћжаc(CO2)ЪЧМзжаЕФ2БЖЃЌЪЧ0.012 molЁЄLЁЊ1 |
| DЃЎЗДгІПЊЪМЪБЃЌБћжаЕФЗДгІЫйТЪзюПьЃЌМзжаЕФЗДгІЫйТЪзюТ§ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
 2Z(g) ЁЂЂк2M(g)
2Z(g) ЁЂЂк2M(g)  N(g)ЃЋP(g)ЗжБ№дкУмБеШнЦїЕФСНИіЗДгІЪвжаНјааЃЌЗДгІЪвжЎМфгаЮоФІВСЁЂПЩЛЌЖЏЕФУмЗтИєАхЁЃЗДгІПЊЪМКЭДяЕНЦНКтзДЬЌЪБгаЙиЮяРэСПЕФБфЛЏШчЭМЫљЪОЃК
N(g)ЃЋP(g)ЗжБ№дкУмБеШнЦїЕФСНИіЗДгІЪвжаНјааЃЌЗДгІЪвжЎМфгаЮоФІВСЁЂПЩЛЌЖЏЕФУмЗтИєАхЁЃЗДгІПЊЪМКЭДяЕНЦНКтзДЬЌЪБгаЙиЮяРэСПЕФБфЛЏШчЭМЫљЪОЃК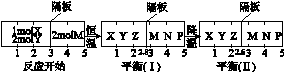
 2Z(g)е§ЗДгІЮЊ ЗДгІЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉДяЕНЦНКт(Ђё)ЪБXЕФзЊЛЏТЪЮЊ ЃЈБЃСєаЁЪ§ЕуКѓСНЮЛЪ§зжЃЌЯТЭЌЃЉЃЛМйЩшЦНКт(Ђё)ЪБзѓБпШнЦїЃЈXЁЂYЁЂZЕФЬхЯЕЃЉЕФЬхЛ§ЮЊ2LЃЌЧѓДЫЮТЖШЯТЕФЛЏбЇЦНКтГЃЪ§
2Z(g)е§ЗДгІЮЊ ЗДгІЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉДяЕНЦНКт(Ђё)ЪБXЕФзЊЛЏТЪЮЊ ЃЈБЃСєаЁЪ§ЕуКѓСНЮЛЪ§зжЃЌЯТЭЌЃЉЃЛМйЩшЦНКт(Ђё)ЪБзѓБпШнЦїЃЈXЁЂYЁЂZЕФЬхЯЕЃЉЕФЬхЛ§ЮЊ2LЃЌЧѓДЫЮТЖШЯТЕФЛЏбЇЦНКтГЃЪ§ ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com