
纯碱和小苏打都是白色晶体,在日常生活中都可以找到。若要在家中将它们区分开来,下面的方法中可行的是
| A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度 |
| B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色 |
| C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀 |
| D.分别放在炒锅中加热,观察是否有残留物 |
科目:高中化学 来源: 题型:单选题
把2.1g的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加
| A.7.2g | B.3.6g | C.2.1 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于Na2CO3和NaHCO3性质的说法正确的是
| A.等浓度时水溶液碱性:NaHCO3>Na2CO3 |
| B.热稳定性:NaHCO3>Na2CO3 |
| C.与盐酸溶液反应的速率(快慢):NaHCO3<Na2CO3 |
| D.向饱和 Na2CO3溶液中通入过量CO2,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知氧化性Fe3+>Cu2+,向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
| A.加入KSCN溶液一定不变红色 |
| B.剩余固体中一定含铜 |
| C.溶液中一定含Cu2+ |
| D.溶液中一定含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在由NaOH、Na2O2组成的化合物中钠元素的质量分数为58%,则混合物中氢元素的质量分数近似为( )
| A.6% | B.2% | C.4% | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关金属及其化合物的说法中正确的是
| A.铝和氢氧化钠溶液反应生成Al(OH)3和H2O |
B.钠在空气中燃烧生成淡黄色的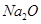 |
| C.铁在高温下与水蒸气反应生成Fe2O3和H2 |
| D.用碳酸钠和氢氧化钙反应制NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100 mL H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液, 产生沉淀的量与所加NaOH溶液的体积的关系如图所示。则原H2SO4物质的量浓度是( )
| A.1mol/L | B.2mol/L | C.3mol/L | D.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O
FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.除去溶液中的Fe2+,可以采用的方法是 ( )
| A.直接加碱,调整溶液pH≥9.6 |
| B.加纯铜粉,将Fe2+还原出来 |
| C.先将Fe2+氧化成Fe3+,再调整pH在3~4 |
| D.通入硫化氢,使Fe2+直接沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com