
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 我国科学家成功研发了甲烷和二氧化碳的共转化技术,利用分子筛催化剂高效制得乙酸,下列有关说法正确的是( )
我国科学家成功研发了甲烷和二氧化碳的共转化技术,利用分子筛催化剂高效制得乙酸,下列有关说法正确的是( )| A. | 消耗22.4 LCO2可制得1mol乙酸 | |
| B. | 该反应过程符合“绿色化学”原理,其原子利用率为100% | |
| C. | 该反应属于取代反应 | |
| D. | 反应物和生成物中均含有极性键和非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 类别 | 物质 |
| A | 碱性氧化物 | Na2O2 Al2O3 MgO |
| B | 酸式盐 | NaHCO3 NaHSO4 NH4Cl |
| C | 弱酸 | H2S H2SO4 CH3COOH |
| D | 强电解质 | AgCl MgSO4 CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
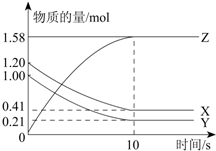
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨作电极电解CuSO4溶液,通电一段时间后,在标准状况下两极产生的气体可能相等 | |
| B. | 船底镶嵌锌块,锌作负极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 电解池中的阳极和原电池中的负极上都发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符号为${\;}_8^{18}$O的原子常用于文物年代的测定 | |
| B. | 原子结构示意图 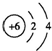 既可以表示12C,也可以表示14C 既可以表示12C,也可以表示14C | |
| C. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S2- | |
| D. | “84消毒液”中有效成分NaClO的电子式为  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
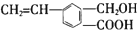 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | 分子式为C10H12O3 | |
| B. | 1 molNa2CO3,最多能消耗l mol有机物M | |
| C. | 1 molM与足量金属钠反应生成11.2 L气体(标准状况) | |
| D. | M能发生取代反应、氧化反应和加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| X | SO2 | CO2 | CO2 | SO2 |
| Y | Cl2 | Cl2 | NH3 | H2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com