
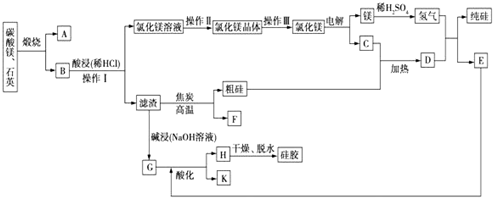
分析 碳酸镁和石英在高温下煅烧,碳酸镁分解生成氧化镁和二氧化碳,则A为CO2,B为MgO和SiO2,加入稀盐酸充分溶解,得到滤渣为SiO2,高温下与C反应生成粗硅和F,F为CO,G为Na2SiO3,H为H2SiO3,氯化镁溶液经蒸发、浓缩、冷却结晶得到氯化镁晶体,经干燥得到氯化镁,电解熔融的氯化镁得到镁和氯气,即C为Cl2,D为SiCl4,E为HCl,则K为NaCl,以此解答该题,
(1)硅胶表面家大,吸附能力强,二氧化碳分子中含有两个碳氧双键;
(2)工业制备粗硅是利用碳还原二氧化硅生成;
(3)分析可知操作Ⅰ是分离固体和溶液用过滤,操作Ⅱ是分离溶液中溶质,蒸发结晶得到溶质晶体;操作Ⅲ是再蒸发皿中蒸发溶液;
(4)氯化镁溶液中镁离子水解生成氢氧化镁沉淀;
(5)溶液G用E酸化是硅酸钠和盐酸反应生成硅酸沉淀;
(6)电极饱和NaCl溶液生成氢氧化钠、氢气和氯气,阳极是氯离子失电子生成氯气.
解答 解:(1)硅胶表面家大,吸附能力强,可用作干燥剂、催化剂的载体,由以上分析可知A为二氧化碳,结构式为O=C=O,
故答案为:干燥剂;催化剂; O=C=O;
(2)工业用二氧化硅和碳在高温下制备粗硅,方程式为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故答案为:SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(3)由以上分析可知操作I为过滤,操作Ⅱ为 蒸发结晶或蒸发浓缩、冷却结晶,操作Ⅲ用于干燥晶体得到固体,所用仪器有铁架台(带铁圈)、酒精灯、蒸发 皿、玻璃棒等,
故答案为:过滤; 蒸发结晶或蒸发浓缩、冷却结晶;蒸发皿、玻璃棒;
(4)加热时氯化镁易水解,为防止水解,应在氯化氢的氛围中进行,
故答案为:防止镁离子水解;
(5)硅酸钠和盐酸反应生成硅酸,反应的方程式为Na2SiO3+2HCl=2NaCl+H2SiO3↓,
故答案为:Na2SiO3+2HCl=2NaCl+H2SiO3↓;
(6)K为NaCl,电解氯化钠溶液生成氢氧化钠、氯气、氢气,离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,阳极生成氯气,方程式为 2Cl--2e-=Cl2↑,
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑; 2Cl--2e-=Cl2↑.
点评 本题考查物质的制备,为高频考点,侧重考查学生知识综合应用能力,明确物质性质及物质分离和提纯方法是解本题关键,知道流程图中各部分可能发生的反应、采用的分离方法,题目难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 在通常情况下氯气比空气重 | |
| B. | 点燃是使氯气和氢气化合的唯一条件 | |
| C. | 氯气跟铁反应生成FeCl2 | |
| D. | 将红热的铜放入氯气中生成蓝色氯化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
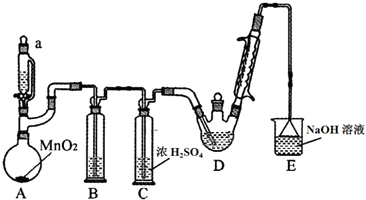
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水,乙醇 | 可溶于水,乙醇,三氯乙醛 | 微溶于水,可溶于乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
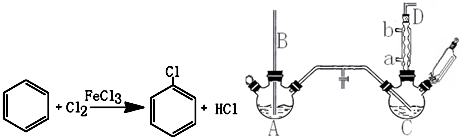
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 200.00mL溶液(黄绿色)$→_{通入适量SO_{2}△}^{(2)还原}$CuCl(白色沉淀)
200.00mL溶液(黄绿色)$→_{通入适量SO_{2}△}^{(2)还原}$CuCl(白色沉淀)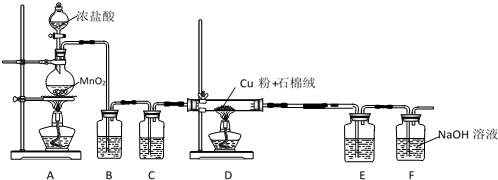
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
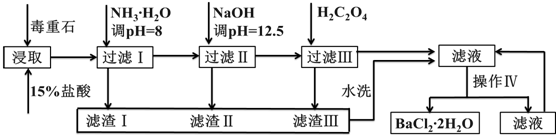
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀的pH | 13.9 | 11.1 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、OH-、NO3-、HCO3- | B. | Na+、Fe3+、Cl-、SCN- | ||
| C. | Na+、Al3+、NO3-、Cl- | D. | K+、Cu2+、SO42-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com