

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:0113 会考题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:实验题


①向甲中通入干燥的Cl2之前,需先通人一段时间CO2,目的是_________________。
②实验过程中,应控制__________,以减少PCl5的生成。
③蒸馏烧瓶乙中得到的粗产品含有POCl3、PCl5等。加入黄磷加热除去 PCl5后,通过___________(填实验操作名称),即可得到PCl3纯品。
(2)已知:
a. H3PO3+H2O+I2 H3PO4+2HI
H3PO4+2HI
b. (NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3
c. Na2S2O3溶液可定量测定碘:I2+2Na2S2O3=Na2S4O6+2NaI
①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取mg产品,水解完全后在500 mL容量瓶中定容;
步骤2:从容量瓶中移取25.00 mL溶液置于碘量瓶中;
步骤3:准确加入c1 mol/L碘溶液V1mL(过量),再________________;
步骤4:_____________;滴至终点时消耗c2 mol/L Na2S2O3溶液V2mL;
②根据上述数据,该产品中PCl3的质量分数为____________(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:0110 模拟题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题

查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:实验题


查看答案和解析>>
科目:高中化学 来源:0116 期中题 题型:实验题


查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题
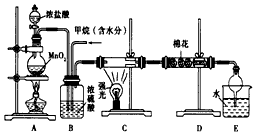
 ,若想理论上获得最多的氯化氢,则x≥__________
,若想理论上获得最多的氯化氢,则x≥__________查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com