
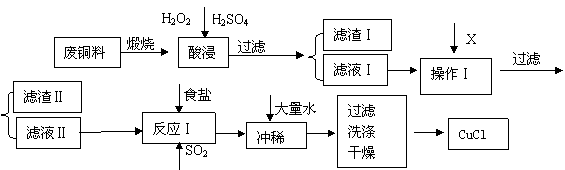
CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是: 。
(2)操作Ⅰ为调节溶液的PH值,范围为 ,加入的物质X可以是( )
A、CuO B、Cu(OH)2 C、NaOH 溶液 D、CaCO3
(3)滤渣Ⅱ的主要成分是 。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式:
。
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是: 。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为: 。
CuOH + H+的平衡常数为: 。
【知识点】物质分离和提纯的方法和基本操作综合应用
【答案解析】(1)使铜转化为可溶于酸的氧化物(2分)
(2)4.7≤PH<5.6 (2分 ) ABC( 2分 )
(3)Fe(OH)3 和 Al(OH)3( 2分 )
(4)2H2O+2Cu2++SO2+4Cl-=2 CuCl2-+ SO42-+4H+ ( 2分 )
(5)提高的CuCl2—生成速率(2分) (6)1(2分)
解析:(1)煅烧的主要目的是使铜转化为可溶于酸的氧化物;
操作Ⅰ的目的是沉淀铁离子和铝离子,还不能沉淀铜离子,所以调节溶液PH值的范围为
4.7≤PH<5.6 ,加入的物质X可以是CuO 、Cu(OH)2 或NaOH 溶液
(3)操作Ⅰ的目的是沉淀铁离子和铝离子,所以滤渣Ⅱ的主要成分是Fe(OH)3 和 Al(OH)3
(4)滤液Ⅱ中含有的离子是Cu2+和Cl-,加入食盐并通入SO2可生成CuCl2-,反应的离子方程式为:2H2O+2Cu2++SO2+4Cl-=2 CuCl2-+ SO42-+4H+
(5)已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,所以温度控制在70~80℃并使用浓NaCl溶液,主要目的是提高的CuCl2—生成速率;
(6)Cu++H2O  CuOH + H+的平衡常数K=C(H+)/C(Cu+),根据沉淀溶解平衡,C(Cu+)=KSP/C(OH-),代入上式,K=C(H+).C(OH-)/KSP=1。
CuOH + H+的平衡常数K=C(H+)/C(Cu+),根据沉淀溶解平衡,C(Cu+)=KSP/C(OH-),代入上式,K=C(H+).C(OH-)/KSP=1。
【思路点拨】本题主要考察常见无机化合物知识,通过所给信息进行加工,书写氧化还原反应方程式,平衡中的有关计算,难度中等。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
某无色透明酸性溶液中,能大量共存的离子组是( )
A.Na+、CO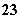 、Cu2+、SO
、Cu2+、SO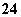 B. K+、Fe3+、SO
B. K+、Fe3+、SO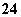 、OH-
、OH-
C. Ca2+、NO3-、Cl-、K+ D.Ba2+、K+、MnO4_、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
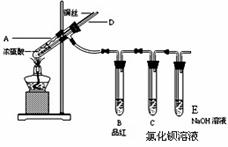 某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
实验1:铜与浓硫酸反应,实验装置如图所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面;
(1)能够证明铜与浓硫酸反应产生的气体的现象: 。
(2)在盛有氯化钡溶液的C试管中除了导管口有气泡外,无其他明显现象,若将其分为两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | __________________________ | __________________________ |
写出其中SO2显示还原性的离子方程式: 。
(3)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,
其原因是: 。
(4)将SO2气体通入含有n mol Na2S溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol。 (不考虑溶解的SO2)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)9.2g氮的氧化物NOx中含有N原子数为0.2 mol,
则NOx的摩尔质量为___________,x数值为_______,
这些质量的NOx在标准状况的体积约为_______。
(2)V L Fe2(SO4)3溶液中含有a g SO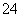 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下表中各项的排布规律,有机物X是按此规律排布的第23项,下列有关X的组成、性质的说法中肯定错误的是
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | CH2O | CH2O2 | CH4O | C2H6 | C2H4O | C2H4O2 | C2H6O |
①是己酸 ②是己醇 ③是戊酸甲酯 ④在稀硫酸中易变质 ⑤一定能与钠反应
A.②⑤ B.①③④
C.③④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修5:有机化学基础】(15分)
白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成:
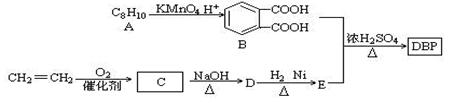
已知以下信息:
①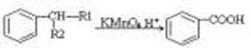
②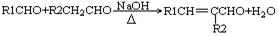
(-R1、-R2表示氢原子或烃基)
(1)A的结构简式 ,D的结构简式是 ,
D→E的反应类型 。
(2)D和H2 1︰1反应生成E,则E官能团名称为_________,DBP的分子式为 .(3)由B和E以物质的量比1︰2合成DBP的化学方程式: 。
(4)写出同时符合下列条件的B的所有同分异构体结构简式 。
①能和NaHCO3溶液反应生成CO2 ③能使FeC13溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
(5)写出B与碳酸氢钠溶液反应的方程式 。
写出C生成D的反应的方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
第3周期元素的基态原子中,不可能出现d电子,主要依据是
A.能量守恒原理 B.泡利不相容原理
C.洪特规则 D.近似能级图中的顺序3d轨道能量比4s轨道高
查看答案和解析>>
科目:高中化学 来源: 题型:
判断同分异构体的种类(不考虑立体异构):
 (1)某烷烃的相对分子质量为114,且分子中含有两个相同的支链,则该烷烃可能的结构共有 种;
(1)某烷烃的相对分子质量为114,且分子中含有两个相同的支链,则该烷烃可能的结构共有 种;
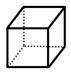
(2)“立方烷”(如图)与氯气发生取代反应,生成的二氯代物共有______种;
(3)甲苯的二氯取代物共有______种;
(4)“金刚烷”(如图),它可看作是由四个等同的六元环组成的空间构型。
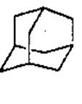 请判断:
请判断:
①一溴代物有 种;
②由氯原子 取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物共有______种。
取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物共有______种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com