
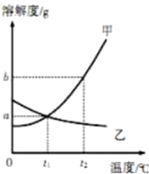
| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时,甲的溶解度为ag | |
| C. | 升高温度,乙的饱和溶液全变成不饱和溶液 | |
| D. | t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数相等 |
分析 A.t1°C后甲的溶解度大于乙,t1°C前甲溶解度小于乙;
B.图象是随温度变化物质溶解度的变化曲线,从图象中读取溶解度;
C.乙的溶解度随温度升高减小,升高温度,乙的饱和溶液析出晶体;
D.t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,乙溶液溶质质量分数不变,甲溶液中溶质质量分数减小.
解答 解:A.甲的溶解度和乙的溶解度大小与温度有关,t1°C后甲的溶解度大于乙,t1°C前甲溶解度小于乙,故A错误;
B.图象是随温度变化物质溶解度的变化曲线,从图象中读取溶解度,t1℃时,甲的溶解度为ag,故B正确;
C.乙的溶解度随温度升高减小,升高温度,乙的饱和溶液析出晶体后仍为饱和溶液,故C错误;
D.t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,乙溶液溶质质量分数不变,甲溶液中会析出晶体,溶质质量分数减小,故D错误;
故选B.
点评 本题考查了物质溶解度随温度的变化特征、注意随温度升高溶解度的变化趋势和溶液饱和程度,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题


 +CH3CH2OH$\stackrel{H+}{→}$
+CH3CH2OH$\stackrel{H+}{→}$ +H2O,
+H2O, ;
; ,则H的结构简式是
,则H的结构简式是 .高聚物L由H通过肽键连接而成,写出生成L的方程式n
.高聚物L由H通过肽键连接而成,写出生成L的方程式n →nH2O+
→nH2O+ (或
(或 ),.
),.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同周期元素的原子电子层数相同 | |
| B. | (长式)元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| C. | 最外层电子数相同的元素都是同一族的元素 | |
| D. | 同一主族元素的原子最外层电子数一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
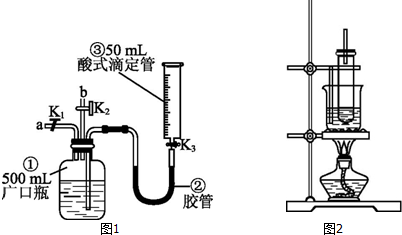
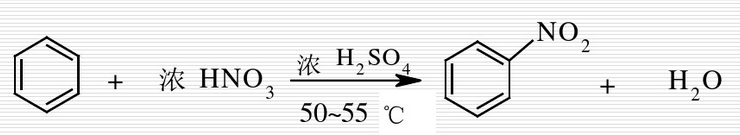 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性强弱:Na>Mg>Al | B. | 热稳定性:Na2CO3>NaHCO3 | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 酸性强弱:HIO4>HBrO4>HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述I | 叙述II |
| A | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙烯可与KMnO4溶液发生反应 | 乙烯具有还原性 |
| D | 乙醇的沸点比乙酸的沸点高 | 乙醇和乙酸可通过蒸馏初步分离 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
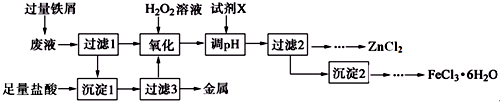
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.2 | 5.4 |
| 完全沉淀pH | 3.7 | 9.6 | 6.9 | 7.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| B. | 用NaOH溶液可以区分HCOOCH3和HCOOCH2CH3 | |
| C. | 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 | |
| D. | 油脂在酸性或碱性条件下均能发生水解反应,且产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O和D2O | B. | ${\;}_{6}^{12}$C和${\;}_{6}^{14}$C | ||
| C. | H2和D2 | D. | O2和O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com