
【题目】下列实验装置或操作与粒子的大小无直接关系的是( )
A. 过滤
过滤
B. 渗析
渗析
C. 萃取
萃取
D.![]() 丁达尔效应
丁达尔效应
【答案】C
【解析】解:A.悬浊液的分散质粒子不能通过滤纸,过滤利用了分散质粒子的大小进行分离,故A错误; B.胶体的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜,渗析利用了分散质粒子的大小进行分离,故B错误;
C.萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系,故C正确;
D.胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应,丁达尔效应与分散质粒子的大小有关,故D错误;
故选:C.
浊液、胶体、溶液的本质区别是分散质粒子的大小不同,悬浊液的分散质粒子不能通过滤纸,浊液的分散质粒子不能透过滤纸,胶体、溶液的分散质粒子能透过滤纸;胶体和浊液的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜;
胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应;
萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系.


科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.100 mol·L-1的NaOH溶液分别逐滴加入到20.00 mL 0.100 0 mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确的是( )
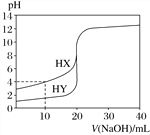
A. V(NaOH)=10.00 mL时,两份溶液中c(X-)>c(Y-)
B. V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
C. V(NaOH)=20.00 mL时,c(OH-)>c(H+)>c(Na+)>c(X-)
D. pH=7时,两份溶液中c(X-)=c(Na+)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BPA的结构简式如右下图所示,常用来生产防碎塑料聚碳酸酯。

(1)该物质的分子式为___________,含氧官能团的名称是_________,属于____类。
(2)该物质最多_____个碳原子共面。
(3)充分燃烧0.1mol该有机物,消耗的O2在标准状况下的体积为_________。
(4)下列关于BPA的叙述中,不正确的是_______。
A.可以发生还原反应
B.遇FeCl3溶液紫色
C.1mol该有机物最多可与2molH2反应
D.可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生实验兴趣小组拟用图1装置气体排液法来完成“NaHCO3和NaCl混合物中NaHCO3含量的测定”的实验.
已知:Na2CO3+CO2+H2O=2NaHCO3 , CO2难溶于饱和NaHCO3溶液.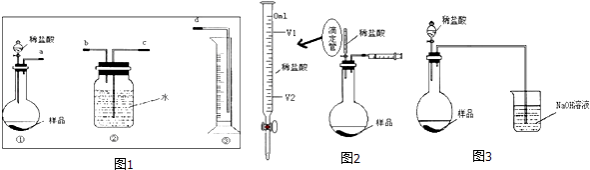
(1)各仪器接口连接顺序是(用接口字母填写).
(2)甲同学认为上述方法误差较大,提出如下改进措施,你认为可行的有 . (填序号)
A.在装置②中水面上滴加少量植物油
B.在装置①中稀盐酸换成稀硫酸,装置②中水换成饱和NaHCO3溶液
C.在装置②中水换成饱和Na2CO3溶液
D.滴加盐酸不宜过快
(3)乙同学认为在装置②③之间的导管内会积存水,使测定结果不准,从而改用图2装置.假定滴定管(用于准确测定滴加液体体积的仪器,其中0刻度在最上面,刻度从上到下依次增大)起始读数为V1mL,终了读数为V2mL,而注射器测定排出的气体为V3mL(标准状况下),混合物样品质量为m g,则原混合物中NaHCO3的质量分数的表达式为(用含V1、V2、V3、m的式子表示).
(4)丙同学改用图3装置,通过测定烧杯中NaOH溶液的增重来确定样品中NaHCO3的含量.你认为乙、丙两同学的方案中,谁的方案更合理 , 理由是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )。
A. Na与水反应时增大水的用量
B. 将铝片改为铝粉,做铝与氧气反应的实验
C. 在K2SO4与BaCl2两溶液反应时,增大压强
D. Fe与稀硫酸反应制取氢气时,改用浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下有关物质的量浓度的叙述正确的是( )
A.等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为1:2:3
B.150 mL 1 mol?L﹣1的氯化钾溶液中的c(Cl﹣)与50 mL 1 mol?L﹣1的氯化铝溶液中的c(Cl﹣)相等
C.20℃时,饱和KCl溶液的密度为1.174 g?cm﹣3 , 物质的量浓度为4.0 mol?L﹣1 , 则此溶液中KCl的质量分数为 ![]() ×100%
×100%
D.20℃时,100 g水可溶解34.2 g KCl,此时KCl饱和溶液的质量分数为34.2%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m__________n(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合亚铜(由[Cu(NH3)2]+和CH3COO-构成)溶液来吸收原料气中的CO气体,其反应的离子方程式为:[Cu(NH3)2]++CO+NH3![]() [Cu (NH3)3CO]+
[Cu (NH3)3CO]+
(1)Cu+基态核外电子排布式________________.
(2)醋酸二氨合亚铜所含元素原子中第一电离能最大的是____________。
(3)写出一种与NH3分子互为等电子体的阳离子_______________。
(4)CH3COO-中碳元素的杂化类型为______________。
(5)1mol [Cu(NH3)3CO]+含有σ键的数目为______________。
(6)N4H4(SO4)2遇碱可生成一种形似白磷的N4分子。画出N4H44+的结构式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器A的名称是________________。安装F中导管时,应选用图2中的_________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O,为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜__________(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是________________________________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_________________________。在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是_________________________________。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_____________,

理由:_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com