
下列说法不正确的是
A.氯水中加少量的Na2CO3粉末,可提高溶液中HC1O的浓度
B.金属单质都具有一定的还原性,金属阳离子都只有氧化性
C.氯气泄漏,自救方法是用湿毛巾或蘸有纯碱溶液的毛巾捂住口鼻并向地势高的地方撤离
D.大气中的N2可作为制硝酸的原料
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:选择题
以下离子检验正确的是( )
A.检验试液中的SO42-:试液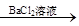 白色沉淀
白色沉淀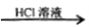 白色沉淀
白色沉淀
B.检验试液中的Cl-:试液 无沉淀
无沉淀 白色沉淀
白色沉淀
C.检验试液中的Fe2+:试液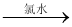 无明显现象
无明显现象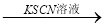 血红色溶液
血红色溶液
D.检验试液中的NH4+ :试液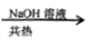 气体逸出
气体逸出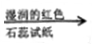 试纸变蓝
试纸变蓝
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
下列各化学术语表达正确的是
A.Na原子结构示意图: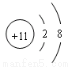
B.乙烷的结构简式:CH3CH3
C.HClO的结构式:H-Cl-O
D.CH4分子的比例模型: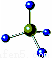
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
在给定条件下,下列加线的物质在化学反应中几乎能被完全消耗的是
A.8.7g二氧化锰与50mL8mol·L-1浓盐酸共热制取氯气
B.19.2g铜与100mL12mol·L-1的硝酸反应
C.常温下,将5.4g铝片投入20mL18mol·L-1的硫酸中
D.将足量的Cu置于50mL18mol·L-1H2SO4溶液中加热
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:填空题
硼镁泥主要成份是MgO(占35%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。从硼镁泥中提取MgSO4·7H2O的流程如下:
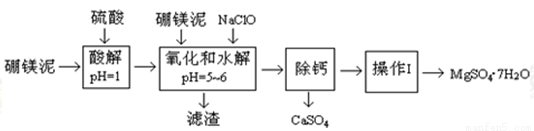
已知:NaClO与Mn2+反应产生MnO2沉淀.
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
开始沉淀pH | 2.3 | 4.0 | 7.6 |
完全沉淀pH | 4.1 | 5.2 | 9.6 |
根据题意回答第(1)~(5)题:
(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施: 、 。
(2)加入的NaClO可与Mn2+反应:Mn2+ + ClO- + H2O = MnO2↓ + 2H+ + Cl-,还有一种离子也会被NaClO氧化,并发生水解,该反应的离子方程式为 。
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3 、MnO2外,还有 。
(4)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤是蒸发浓缩, 。“操作I”是将滤液继续蒸发浓缩,冷却结晶, __________ ,便得到了MgSO4·7H2O。
(5)实验中提供的硼镁泥共100 g,得到的MgSO4·7H2O为172.2 g,计算MgSO4·7H2O的产率为 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:选择题
分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是( )
A.N2O、Na2O2、CaO·SiO2均含有氧元素,都是氧化物
B.HClO、浓硫酸、HNO3均具有氧化性,都是氧化性酸
C.HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.NaBr、MgO、AlCl3均由活泼金属和活泼非金属化合而成,都是离子化合物
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.Fe2O3溶于HI溶液中:Fe2O3 + 6H+ =2Fe3++ 3H2O
B.碳酸钠的水【解析】
CO32-+ 2H2O H2CO3 + 2OH-
H2CO3 + 2OH-
C.硫酸铝溶液中滴加过量浓氨水:Al3++4NH3·H2O===AlO +4NH4++2H2O
+4NH4++2H2O
D.用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+ =I2 +2H2O
查看答案和解析>>
科目:高中化学 来源:2016届广西柳州铁路第一中学高三上学期10月月考理化学试卷(解析版) 题型:填空题
氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)室温下,浓度均为0.1mol/L的亚硝酸(HNO2)、次氯酸两种溶液,它们的电离常数Ka分别为:7.1×10﹣4、2.98×10﹣8。将0.1mol/L的亚硝酸稀释,c(H+)将 (填“不变”、“增大”、“减小”);Ka值将(填“不变”、“增大”、“减小”) 。写出涉及HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的化学方程式 。
(2)羟胺(NH2OH)可看成是氨分子内的l个氢原子被羟基取代的产物,常用作还原剂,其水溶液显弱碱性。已知NH2OH在水溶液中呈弱碱性的原理与NH3在水溶液中相似,请用电离方程式表示其原因 。
(3)磷及部分重要化合物的相互转化如图1所示。

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是 。
②不慎将白磷沾到皮肤上,可用CuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol CuSO4所能氧化的白磷的物质的量为 mol。
(4)若处理后的废水中c(PO43﹣)=4×10﹣7 mol•L﹣1,溶液中c(Ca2+)= mol•L﹣1。(已知Ksp[Ca3(PO4)2]=2×10﹣29)
(5)某液氨﹣液氧燃料电池示意图如图2,该燃料电池的工作效率为50%,现用作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液中NaOH的浓度为0.3mol•L﹣1,则该过程中需要氨气的质量为 g。(假设溶液电解前后体积不变)
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
下列图①②③原子结构模型中依次符合卢瑟福、道尔顿、汤姆生的观点的是
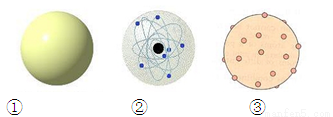
A.①②③ B.③①②
C.③②① D.②①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com