
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:
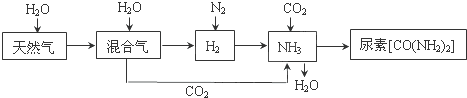
| ||
| ||
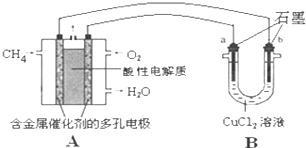
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江嵊泗中学高二下学期第二次月考化学卷(7、8班)(解析版) 题型:填空题
氰酸(化学式:HOCN)是一种有挥发性和腐蚀性的液体,在水中立刻发生如下反应形成盐X(俗名碳铵):HOCN + 2H2O → X。
(1). 在上述反应所涉及的各元素中,半径最大的元素原子在周期表中的位置是___________,该原子核外电子共占据_______个轨道。
(2). X所含阳离子的电子式是________;已知25℃时0.1mol/L X溶液pH =7.8,用离子方程式表示原因:______________________。
(3). 能说明氮元素的非金属性比碳元素强的事实是_________(选填编号)。
a. 共用电子对偏向:H-N>H-C b. 氧化性:NO2>CO2
c. 酸性:HNO3>H2CO3 d. 沸点:NH3>CH4
(4). 据测定,氰酸有两种结构,一种分子内含有叁键,称为正氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出正氰酸和异氰酸的结构式:_______________、______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com