
| A. | ②③④ | B. | ①③④ | C. | ②③④ | D. | ③④⑤ |
分析 ①碳酸比硝酸弱,与硝酸钡不反应;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应:Ca(OH)2+2CO2═Ca(HCO3)2;
③碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应生成硅酸沉淀;
④NaAlO2溶液通入过量的二氧化碳,可生成氢氧化铝沉淀;
⑤过量的CO2通入饱和Na2CO3溶液中发生反应生成碳酸氢钠;
解答 解:①碳酸比硝酸弱,二氧化碳与Ba(NO3)2溶液不反应,没有沉淀生成,故①错误;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应:Ca(OH)2+2CO2═Ca(HCO3)2,无沉淀生成,故②错误;
③碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应:2CO2+Na2SiO3+2H2O═2NaHCO3+H2SiO3↓,产生硅酸沉淀,故③正确;
④NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H2O+NaAlO2+CO2=Al(OH)3↓+NaHCO3,故④正确;
⑤过量的CO2通入饱和Na2CO3溶液中发生反应:Na2CO3+H2O+CO2═2NaHCO3↓,因为碳酸氢钠溶解度比碳酸钠小,所以有NaHCO3晶体析出,故⑤正确;
故选D.
点评 本题考查了元素及其化合物的性质等,侧重于元素化合物知识的综合理解和运用的考查,比较基础,注意基础知识的掌握,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{78}^{202}$Pt原子核中含有78个中子 | |
| B. | ${\;}_{78}^{202}$Pt原子核外有124个电子 | |
| C. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同素异形体 | |
| D. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结构相似的分子晶体的溶沸点,与相对分子质量呈正相关,所以HF<HCl | |
| B. | Na、Mg、Al原子最外层电子数依次增多,原子半径也依次增大 | |
| C. | 在分子中,两个原子间的键长越长,键能越大 | |
| D. | 一般而言,晶格能越高,离子晶体的熔点越高、硬度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有氧元素的化合物都是氧化物 | |
| B. | 同种分子构成的物质一定是纯净物 | |
| C. | 非金属氧化物都是酸性氧化物 | |
| D. | BaSO4在水溶液中难导电.所以BaSO4是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH═CH3COO-+H+ | B. | NaHCO3?Na++H++CO32- | ||
| C. | H2CO3?2H++CO32- | D. | H2SO4═2H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
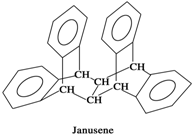 如图是一种形状酷似罗马两面神Janus的有机物结构简式,化 学家建议将该分子叫做“Janusene”,下列说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式,化 学家建议将该分子叫做“Janusene”,下列说法正确的是( )| A. | Janusene的分子式为C30H20 | |
| B. | Janusene属于苯的同系物 | |
| C. | Janusene苯环上的一氯代物有4种 | |
| D. | Janusene既可发生氧化反应,又可发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com