
【题目】化学与生活密切相关,下列应用中一定发生了氧化还原反应的是
A.食醋除去水壶的水垢B.氯气作自来水的消毒剂
C.二氧化硫漂白草帽D.石膏点豆腐
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
【题目】氮化镁(Mg3N2)在工业上具有非常广泛的应用。某化学兴趣小组用镁与氮气反应制备Mg3N2并进行有关实验。实验装置如下所示:
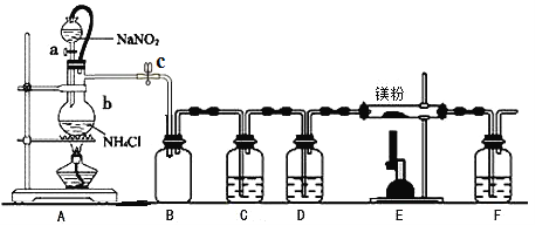
已知:①氮化镁常温下为浅黄色粉末,极易与水反应。
②亚硝酸钠和氯化铵制取氮气的反应剧烈放热,产生氮气的速度较快。
③温度较高时,亚硝酸钠会分解产生O2等。
回答下列问题:
(1)仪器b的名称是________,写出装置A中发生反应的化学方程式___________________。
(2)某同学检验装置A部分的气密性,关闭止水夹c后,开启活塞a,水不断往下滴,直至全部流入烧瓶。试判断:A部分装置是否漏气?________(填“漏气”、“不漏气”或“无法确定”),判断理由:____________。
(3)装置C中为饱和硫酸亚铁溶液,作用是___________,F装置的作用是_______________________。
(4)加热至反应开始发生,需移走A处酒精灯,原因是_______________________________________。
(5)反应结束后,取m g E中样品于试管中,加足量蒸馏水,得V mL气体(换算为标准状况),则样品中氮化镁的质量分数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】腐乳是桂林有名的特产之一,请参考图中的有关信息回答下列问题。

(1)制作腐乳的主要原料是黄豆,黄豆富含人体所需的营养物质主要是_______。制作腐乳用到了加碘盐,即在食盐中加入_______(写出碘化合物的名称或化学式)。
(2)腐乳在酿制过程中会产生多种氨基酸,故味道鲜美,这些氨基酸的通式为________。腐乳虽好但不能作为主食,原因在于腐乳所含的_______类营养素较少,而该类营养素是人类生命活动所需能量的主要来源物质。
(3)盛装腐乳的陶罐属于_______(填“无机”或“有机”)非金属材料制品,陶罐的主要成分为_______酸盐。
(4)外包装纸盒所用纸的主要成分是____________。包装盒提绳的主要成分是聚丙烯塑料,由丙烯合成聚丙烯的化学方程式为:_____________________________。
(5)聚丙烯等材料制成的塑料制品不应随意丢弃,以免造成俗称“_________污染”的环境问题。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是现行中学化学教科书中元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题。
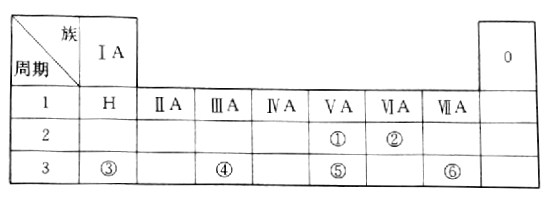
(1)② 表示的元素是______(填元素符号);
(2)①、⑤两种元素的原子半径大小为①______⑤(填“< ”或“>”);
(3)③、④两种元素的金属性强弱顺序为:③______④(填“< ”或“>”);
(4)写出③与⑥两种元素所形成化合物的化学式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示:
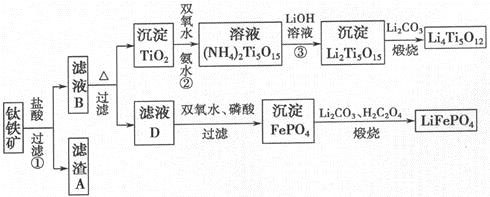
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl—= Fe2++ TiOCl42—+2H2O
(1)化合物FeTiO3中铁元素的化合价是_______。
(2)滤渣A的成分是_______。
(3)滤液B中TiOCl42-和水反应转化生成TiO2的离子方程式是_______ 。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15 溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因_ 。
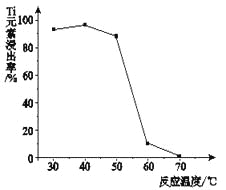
(5)反应③的化学方程式是 。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是_______。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:
Li4Ti5O12+ 3LiFePO4![]() Li7Ti5O12+ 3FePO4 该电池充电时阳极反应式是: 。
Li7Ti5O12+ 3FePO4 该电池充电时阳极反应式是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化钠固体易吸收空气中的二氧化碳而变质。取4.65 g已部分变质的氢氧化钠固体与36.5 g 10%的盐酸恰好完全反应后,将溶液蒸干,所得固体的质量是( )
A. 11.7 g B. 5.85 g C. 4.65 g D. 8.3 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D.步骤(2)产物中残留的丙烯醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.工业合成氨是一种人工固氮方法B.侯氏制碱法应用了物质溶解度的差异
C.播撒碘化银可实现人工降雨D.铁是人类最早使用的金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】感光性高分子也称为“光敏性高分子”,是一种在彩电荧光屏及大规集成电路制造中应用较广的新型高分子材料.其中一种的结构简式为: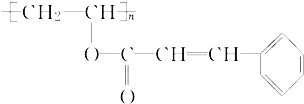 。试回答下列问题:
。试回答下列问题:
(1)已知它是由两种单体经酯化后聚合而成的,试推断这两种单体的结构简式_________________;
(2)写出由(1)中两种单体生成高聚物的化学反应方程式:
①_________________________________________________________________;
②_________________________________________________________________;
(3)对此高聚物的性质判断不正确的是__________(填字母).
A.在酸性条件下可以发生水解
B.此高聚物不能使溴水褪色
C.此高聚物可以使酸性高锰酸钾溶液褪色
D.此高聚物可与液溴发生取代反应.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com