
A��J���ճ������г��������ֽ����������ֽ�����NaOH���ԭ��أ�A��������F�����������嵥�ʣ������������µ�ת����ϵ�����ֲ��P������ȥ�����ش����⣺
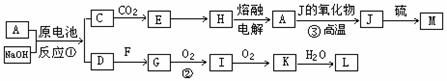
��1��д����ԭ��ص��ܷ�Ӧ����ʽ ��
��2��д���ڵĻ�ѧ����ʽ ��
��3������ʱpH=12��C��Һ�У����ʵ������������ʵ�������Ũ��֮��Ϊ ����д������ʽ��
��4��������J��������Ϊ�����������ÿ����1mol J�ų�QkJ����������д��A��J��Ӧ���Ȼ�ѧ����ʽ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й��Ȼ�ѧ����ʽ��������ȷ����
| A | ��֪2H2O��g��= 2H2��g��+O2��g�� ��H=+483.6 kJ/mol����������ȼ����Ϊ ��H=��241.8kJ/mol | |
| B�� | ��֪C��ʯī��s��= C�����ʯ��s�� ��H��0������ʯ����ʯī�ȶ� | |
| �� | C�� | ��֪�к���Ϊ��H =��57.3kJ/mol����ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ�� NaOH��aq��+ CH3COOH��aq��= CH3COONa��aq��+ H2O��l����H=��57.3kJ/mol |
| �� | D�� | ��֪2C(s)+ 2O2(g) = 2CO2 (g) ��H1�� 2C(s)+ O2 (g) = 2CO(g) ��H2�����H1����H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
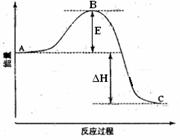
2SO2(g)+O2(g) =2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2(g)����Ϊ1mol SO3(g)�Ħ�H= ��99kJ��mol-1����ش��������⣺
��1��ͼ��A��ʾ ��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ�� ����С����ޡ���Ӱ�졣�÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�� ������ߡ����ǡ����͡�������H (��������С�����䡱)��������
��2����֪�������ȼ����Ϊ296 KJ��mol-1��������S(s)����3 molSO3(g)�ġ�H��Ҫ�������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2mol��L-1�������2mol��L-1����������Һ10mL�У�����0.96gͭ�ۣ���ַ�Ӧ�������ռ�������µ���������Ϊ
A.89.6mL B.112mL C.168mL D.224mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�������ȷ�����������ϵ����
| ѡ�� | ������ | ������ |
| A | SO2��Ư���� | SO2��ʹ��ˮ��ɫ |
| B | Si�е����� | SiO2�������ƹ��ά |
| C | Ũ������ǿ������ | Ũ��������ڸ���H2��CO |
| D | Fe3+�������� | FeCl3��Һ�������ܽ���վɵ�·���е�ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����Լ������ʢ�ŷ�����ȷ����(����)
A��Ũ����ʢ����ͭ��������
B��ϡ����ʢ��������������
C��NaOH��Һ�����ڴ��������Լ�ƿ��
D��NaOH��Һ�����ڴ����������Լ�ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Na2O2��CO2�ķ�Ӧ�У��������뻹ԭ������������(����)
A��1��1 B��2��1 C��1��2 D��8��53
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����������ת����
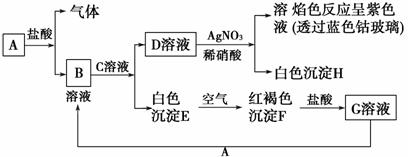
�Իش�
(1)д��B�Ļ�ѧʽ__________�� D�Ļ�ѧʽ__________��
(2)д����Eת���F�Ļ�ѧ����ʽ_______________________��
(3)д����KSCN����G����__________________����G��Һ����A���й����ӷ�Ӧ����ʽ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�˼��������̼�Ƿ��������ƿ����ȷ�ķ����ǣ� ��
A. �������ʯ��ˮ B. ������ɫʯ����Һ
C. ��ȼ�ŵ�ľ������ƿ�� D. ��ȼ�ŵ�ľ��Ѹ������ƿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com