
| A. | 1 | B. | 4 | C. | 3 | D. | 8 |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
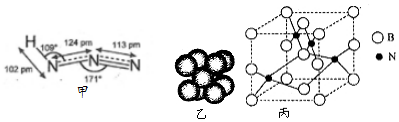
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NCl3 的沸点高于 NH3 的沸点 | |
| B. | 在氨水中,大部分 NH3 与 H2O 以氢键(用“…”表示)结合形成 NH3•H2O 分子,则NH3•H2O 的结构式为 | |
| C. | NCl3 分子是非极性分子 | |
| D. | NBr3 比 NCl3 易挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液与盐酸发生中和反应 OH-+H+═H2O | |
| B. | 氢氧化钡溶液与硫酸溶液发生中和反应 2OH-+2H+═2H2O | |
| C. | 稀盐酸滴在大理石上 CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向氯化钠溶液中滴加硝酸银溶液 Cl-+Ag+═AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn和H2SO4的总能量大于ZnSO4和H2的总能量 | |
| B. | 反应过程中能量关系可用如图表示 | |
| C. | 若将该反应设计成原电池,则Zn为负极 | |
| D. | 若将该反应设计成原电池,当有32.5g锌溶解时正极放出11.2L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| B. | 用氢氧化钠溶液除去镁粉中的铝粉:2Al+2OH-+3H2O═2【Al(OH)4】-+H2↑ | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-═NH3↑+H2O | |
| D. | 将食醋与“84”消毒液混合产生黄绿色气体:2H++Cl-+ClO-═Cl2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com