
【题目】托盘天平的两个托盘上各放一只相同的烧杯,再分别向两烧杯中放入等质量、等质量分数且足量的稀硫酸,调节天平至平衡。然后,向一只烧杯中加入一定质量的镁,向另一烧杯中加入等质量的铜、铝合金,反应后天平仍然保持平衡。则该合金中铜与铝的质量比为( )
A. 64∶27B. 8∶3C. 3∶1D. 1∶3
【答案】D
【解析】
稀硫酸质量相等,加入金属的质量相等,反应后太平仍然保持平衡,则两侧托盘中质量增重相等,令Mg的质量为24g,根据方程式计算质量差,令Al的质量为x,再根据2Al+3H2SO4═Al2(SO4)3+3H2↑,表示出生成氢气质量,利用增重列方程计算Al的质量,进而计算Cu的质量,据此解答。
令Mg的质量为24g,则:
Mg+H2SO4═MgSO4+H2↑ 质量增重
24 2 22
24g 22g
设Al的质量为x,则:
2Al+3H2SO4═Al2(SO4)3+3H2↑
2×27 2×3
x ![]() x
x
故24g-![]() x=22g,解得x=18g,
x=22g,解得x=18g,
故Cu的质量=24g-18g=6g,该合金中铜与铝的质量比=6g:18g=1:3。
故选D。


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】取50mL0.3mol/L的硫酸注入250mL容量瓶中,加水稀释至刻度线,则该溶液中的H+的物质的量浓度为
A. 0.06mol/L B. 0.12 mol/L C. 0.24mol/L D. 0.03mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A为原料合成F,其合成路线如图所示:

(1)写出决定B、D性质的重要原子团的名称:
B________、D________。
(2)A的结构式为____________。
(3)写出下列反应的化学方程式并注明反应类型:
①______________________,反应类型:_______;
②_________________,反应类型:________。
(4)实验室怎样区分B和D?___________。
(5)除去F中少量B和D的最好试剂是________(填字母)。
A 饱和碳酸钠溶液 B 氢氧化钠溶液 C 苯 D 水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是:
A. ![]() 和
和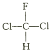 为同种物质
为同种物质
B. 15g甲基(﹣CH3)含有的电子数是7NA
C. 7.8g苯中含有的碳碳双键数为0.3NA
D. 标准状况下,2.24 L CCl4中的原子总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照要求将相应序号填入空白中:
①![]() ②金刚石 ③CO ④CO2 ⑤37Cl ⑥
②金刚石 ③CO ④CO2 ⑤37Cl ⑥![]() ⑦SO2 ⑧
⑦SO2 ⑧![]() ⑨石墨
⑨石墨
其中________互为同位素,______为酸性氧化物,_____的质量数相等,但不能互为同位素,_______互称同素异形体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元索对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 原于半径:r(Y)>r(Z)>r(W)
B. 化合物N、乙烯使溴水褪色的原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按反应N2H5++4Fe3+……→4Fe2++Y+……,在水溶液中N2H5+离子将Fe3+还原为Fe2+,作为N2H5+离子的氧化产物Y可能为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用反应Cr2O7n-+CH3OH+H+→Cr3++CO2↑+H2O(未配平)来测定工业甲醇中甲醇的含量,下列说法中正确的是( )
A. 溶液的颜色从灰绿色变为橙色
B. Cr2O7n-发生氧化反应
C. 若配平后Cr3+和CO2的化学计量数比为2:1,则Cr2O7n-中的n=2
D. 若有3.2 g CH3OH参加反应,则转移的电子数为6.02×1022
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.1molCu(OH)2后,恰好使溶液恢复到电解前的浓度。则电解过程中转移的电子的物质的量为
A.0.4molB.0.5molC.0.6molD.0.8mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com