
����Ŀ��ijʵ��С���������ͼװ�öԽ�̿��ԭ����������������ijɷֽ���̽���� 
��֪��PdCl2��Һ�����ڼ���CO����Ӧ�Ļ�ѧ����ʽΪCO+PdCl2+H2O�TCO2+2HCl+Pd����������ɫ�����ٷ�ĩ��ʹ��Һ����ǣ���
��1��ʵ�����Ҫ�������£� �ٵ�ȼ�ƾ����
�ڼ��װ�õ�������
��ͨ��N2һ��ʱ��
����A��Ӳ�ʲ�������װ�뽹̿��������������������ﹲm g����ȷ�IJ���˳���� ��
��2��ʵ��ʱҪͨ���㹻��ʱ���N2 �� ��ԭ���� ��
��3��װ��D����ʢ�Լ�Ϊ������ţ�
A.NaOH��Һ
B.Ca��OH��2��Һ
C.PdCl2��Һ
D.ϡH2SO4��Һ
��4����װ��C��D����Һ������ǣ��Ҿ�����������������ʵ�����ȣ���A�з�Ӧ�Ļ�ѧ����ʽΪ �� ʵ�������Cװ������ng����m g�������SiO2���������� ��
���𰸡�
��1���ڢܢۢ�
��2��Ҫ�õ�����װ���еĿ����ž�����������е�������������̼��ˮ������ʵ���������
��3��C
��4��3SiO2+4C ![]() 2CO2+2CO+3Si��
2CO2+2CO+3Si��![]() ��100%
��100%
���������⣺��1��ʵ�鲽��Ϊ�ڼ��װ�õ������ԣ�����A��Ӳ�ʲ�������װ�뽹̿��������������������ﹲm g����ͨ��N2һ��ʱ�䣬�ٵ�ȼ�ƾ���ƣ���ȷ�IJ���˳��Ϊ���ڢܢۢ٣����Դ��ǣ��ڢܢۢ٣���2��̼��������跴ӦҪ�ڸ����½��У���������̼�������������Ӧ������ʵ��ʱҪ��װ���еĿ����ž�������ʵ��ʱҪͨ���㹻��ʱ���N2 �� ���Դ��ǣ�Ҫ�õ�����װ���еĿ����ž�����������е�������������̼��ˮ������ʵ��������ţ���3������Ԫ���غ㣬̼��������跴Ӧ��������һ����̼Ҳ�������ɶ�����̼������Cװ������������û�ж�����̼��Dװ����������һ����̼��������C��D����ʢ�Լ��ֱ�Ϊ����ʯ��ˮ��PdCl2��Һ��
���Դ��ǣ�C����4����װ��C��D����Һ������ǣ�˵�����ж�����̼����һ����̼������������������ʵ�����ȣ�����Ԫ���غ��֪��ѧ����ʽΪ3SiO2+4C ![]() 2CO2+2CO+3Si��
2CO2+2CO+3Si��
ʵ�������Cװ������ngΪ���յĶ�����̼�������������������ʵ�����ȼ���õ�һ����̼�Ͷ�����̼���ʵ�����
n��CO2��=n��CO��= ![]() =
= ![]() mol��
mol��
3SiO2+4C | 2CO2+2CO+3Si |
3 | 2 |
n |
|
n= ![]() mol��
mol��
����������������= ![]() ��100%=
��100%= ![]() ��100%��
��100%��
���Դ��ǣ�3SiO2+4C ![]() 2CO2+2CO+3Si��
2CO2+2CO+3Si�� ![]() ��100%
��100%



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�Ԫ�����ڱ���˵���д�����ǣ� ��
A. Ԫ�����ڱ��е�16������Ϊ��A��
B. ��A��Ԫ��Ҳ��Ϊ±��Ԫ��
C. Ԫ�����ڱ��У����������8��9��10��������
D. 0��Ԫ�ص�ԭ��������������Ϊ8��Ԫ�ػ��ϼ�Ϊ0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±�����ش�
ʵ���� | HA���ʵ���Ũ�ȣ�molL��1�� | NaOH���ʵ���Ũ�ȣ�molL��1�� | �����Һ��pH |
�� | 0.2 | 0.2 | pH=a |
�� | c | 0.2 | pH=7 |
�� | 0.2 | 0.1 | pH��7 |
�� | 0.1 | 0.1 | pH=9 |
��1���������������ʵ���������Ӽ��������������a��˵��HA��ǿ�ỹ�����ᣬ��a7����HA��ǿ���a7����HA�����ᣨ�������=����
��2���������������ʵ�����������������������c�Ƿ�һ������0.2��ѡ��ǡ��������Һ������Ũ��c��A������ c��Na+���Ĵ�С��ϵ�� ��
��3������ʵ����������HA���ᣨѡ�ǿ�������������û����Һ������Ũ���ɴ�С��˳���� ��
��4������ʵ�����û����Һ����ˮ�������c��OH����=molL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ͷ�����������������Һ�г�ַ�Ӧ�������й����û����Һ��������ȷ���ǣ� �� 
A.����Һ�У�Ag+��K+��NH4+��SO42�����Դ�������
B.����Һ�У�Na+��OH����NO3����CO32�����ܴ�������
C.�����Һ����μ���AlCl3��Һ�����ɳ��������AlCl3��Һ��ϵ��ͼ
D.�����Һ����μ���ϡ���ᣬ���ɳ��������ϡ�����ϵ��ͼ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ����ұ���������ϩ�� ![]() ������˵����ȷ���ǣ� ��
������˵����ȷ���ǣ� ��
A.�÷�Ӧ������Ϊ��ȥ��Ӧ
B.�ұ���ͬ���칹�干������
C.����Br2��CCl4�����ұ��ͱ���ϩ
D.�ұ��ͱ���ϩ�����ڹ�ƽ���̼ԭ������Ϊ7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ������ʵ�������ȷ���ǣ� ��
A. ����������Ӧʱ��������������������������
B. �����ڿ��������ȿ����ۻ��һᷢ������ȼ��
C. ������ǽ���������Ӧʱ����������һ���ǽ���
D. ��˿�����ڿ����л����д������ж�����ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��������ʾij��ø�ڸ����¶���ø����������ø���Եİٷֱȣ��������ǽ�����ø�ڲ�ͬ�¶��±����㹻����ʱ�䣬����ø������ߵ��¶��²������ø���ԣ��ɴ˵õ�ø�����ȶ������ݡ���ش��������⣺

��1���̶���ø�ij��÷�����________________��
��2���������У�35����90�������ݵ�����______________��ʱ��õġ�
��3������ø�̶���������������������¶ȷ�Χ��_______________��ԭ����______________��
��4���о������мס������������ܽ�����ø�Ĵ�Ч�ʡ���֪��ø���ĵ���Ũ�ȱ仯��ı�����ʶ�ø��Ӱ�죬������ı������ʶ�ø��Ӱ�졣��ͼһ�ǽ���ø���Ե����ֻ���ģ�ͣ�ͼ����������ø�Ļ��Բ�������ʱ����ʼ��Ӧ���������Ũ�ȵĹ�ϵ��

�����ϼס������ʶ�øӰ���ģ�ͷֱ���______________��_______________��
�����ڴ����ָ��λ�û������������ʱ����ʼ��Ӧ���������Ũ��֮��Ĺ�ϵ���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ�������ж���ȷ���ǣ� ��
A.1 g H2���е���ԭ����ĿΪ2NA
B.���³�ѹ�£�22.4 L O2���еķ�����ĿΪNA
C.1 L 1 molL��1 KOH��Һ�к��еļ�������ĿΪNA
D.1 mol Zn��ΪZn2+ʧȥ�ĵ�����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����Ƴ���ͼ��ʾװ�����Ľ��̲��С�ͭ�����ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ���� 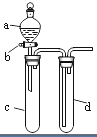
��1��ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c����Ŀ���� ��
��2����d�м�����NaOH��Һ��c�з�һС��ͭƬ���ɷ�Һ©��a��c�м���2mLŨ���ᣬc�з�Ӧ�Ļ�ѧ����ʽ�� ��
���� | ��Ӧ�� |
�� | Cu��ŨHNO3 |
�� | Cu��ϡHNO3 |
�� | Cu��O2��ϡHNO3 |
��3���±�����ȡ����ͭ�����ַ�������������ɫ��ѧ�������ѷ����� ��
��4����С�黹������װ�ý���ʵ��֤�����ԣ�HCl��H2CO3��H2SiO3 �� ���Һ©��a�м�����Լ��� �� c�м�����Լ��� �� d�м�����Լ�����ʵ������Ϊ �� ����ʵ����ڲ���֮�����Ľ��Ĵ�ʩ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com