

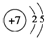 ;
;分析 短周期元素A、B、C、D、E,①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜,则A为Al元素;②B元素的原子序数比A元素大,B处于第三周期,其原子的次外层的电子数是最外层电子数的$\frac{4}{3}$倍,则最外层电子数为8÷$\frac{4}{3}$=6,故B为S元素;③E与B同主族,则E为O元素;周期表中C原子的原子半径最小,则C为H元素;D与C形成DC3,为三角锥型结构,D的单质通过三键形成的双原子分子,结合反应可知,D为氮元素,据此解答.
解答 解:短周期元素A、B、C、D、E,①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜,则A为Al元素;②B元素的原子序数比A元素大,B处于第三周期,其原子的次外层的电子数是最外层电子数的$\frac{4}{3}$倍,则最外层电子数为8÷$\frac{4}{3}$=6,故B为S元素;③E与B同主族,则E为O元素;周期表中C原子的原子半径最小,则C为H元素;D与C形成DC3,为三角锥型结构,D的单质通过三键形成的双原子分子,结合反应可知,D为氮元素,
(1)氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
(2)B为S元素,处于元素周期表中第三周期第ⅥA族,B的氧化物为二氧化硫、三氧化硫,均含有共价键,故答案为:三;ⅥA;共价键;
(3)D为氮元素,原子核外有7个电子,原子结构示意图为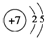 ,故答案为:
,故答案为: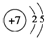 ;
;
(4)非金属性S<O,故氢化物稳定性:H2O>H2S,故答案为:H2O;H2S;
(5)氮气与氢气在工业上常用由于合成氨,反应方程式为:N2+3H2 $\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$ 2NH3,故答案为:N2+3H2 $\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$ 2NH3.
点评 本题考查结构性质位置关系,推断元素是解题关键,难度不大,有利于基础知识的巩固.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②④ | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-CH2-CH2Br | B. | CH2═CH-CH2-CH2-CH2Cl | ||
| C. | CH3Cl | D. | CH2═CH-CH2-C(CH3)2CH2Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m=2,n=4 | B. | m=0.5,n=4 | C. | m=2,n=0.25 | D. | m=0.5,n=0.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提倡绿色生活,使用公共交通 | |
| B. | 大力发展火电,缓解用电紧张 | |
| C. | 开发太阳能、风能、氢能等清洁能源 | |
| D. | 研制出性能优良的催化剂,降低反应所需温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KOH | B. | H2SO4 | C. | HClO4 | D. | MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 具有抗癌作用,而
具有抗癌作用,而 没有抗癌作用,对此下列有关叙述正确的是( )
没有抗癌作用,对此下列有关叙述正确的是( )| A. | 两者互为同分异构体,都是以Pt原子为中心的四面体结构 | |
| B. | 两者互为同分异构体,都是以Pt原子为中心的平面结构 | |
| C. | 两者为同一物质,都是以Pt原子为中心的四面体结构 | |
| D. | 两者为同一物质,都是以Pt原子为中心的平面结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验室中一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样(如图所示).已知固体M只可能是Na2S、Na2SO3、Na2SiO3、Na2SO4中的一种.若取少量固体M配成稀溶液进行有关实验,下列说法不正确的是( )
实验室中一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样(如图所示).已知固体M只可能是Na2S、Na2SO3、Na2SiO3、Na2SO4中的一种.若取少量固体M配成稀溶液进行有关实验,下列说法不正确的是( )| A. | 只用盐酸一种试剂就可以确定该固体M的成分 | |
| B. | 往溶液中加入稀硝酸酸化的BaCl2溶液,若有白色沉淀生成,则固体M为Na2SO4 | |
| C. | 往溶液中通入二氧化碳,若有白色沉淀生成,则固体M为Na2SiO3 | |
| D. | 只用氯水一种试剂就可以确定该固体M的成分 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com