
| 催化剂 |
| △ |
| 改变条件 | 速率变化 | |
| ① | 降低温度 | ______ |
| ② | 增加O2浓度 | ______ |
| ③ | 使用V2O5做催化剂 | ______ |
| ④ | 压缩气体 | ______ |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:不详 题型:单选题
 3C(g)+D(s)(正反应为放热反应),图2-28中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )
3C(g)+D(s)(正反应为放热反应),图2-28中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是( )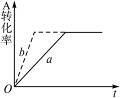
| A.增大A的浓度 | B.扩大容器的容积 |
| C.加入催化剂 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 1 |
| 2 |
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时减小压强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
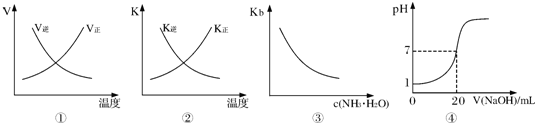
| A.图①表示反应N2(g)+O2(g)?2NO(g)△H>0正、逆反应的速率随温度的变化 |
| B.图②表示反应N2(g)+3H2(g)?2NH3(g)△H<0正、逆反应的平衡常数随温度的变化 |
| C.图③表示氨水的电离平衡常数随氨水浓度c(NH3?H2O)的变化 |
| D.图④表示25℃时,用0.1mol?L-1NaOH溶液滴定20mL 0.lmol?L-1盐酸,溶液的pH随加入碱体积的变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 实验序号 | 铁的质量/g | 铁的形态 | c(H2SO4) /mol?L-1 | V(H2SO4) /mL | 溶液温度 | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 铁片 | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | 铁片 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 铁粉 | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | 铁片 | 1.0 | 50 | 20 | 35 | 125 |
| 5 | 0.10 | 铁片 | 1.0 | 50 | 35 | 50 | 20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤ | B.②③④⑤ | C.①③④⑤ | D.①②④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.缩小体积使压强增大 |
| B.体积不变充入N2使压强增大 |
| C.体积不变充入H2使压强增大 |
| D.压强不变充入稀有气体氖 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,下列说法中不正确的是( )
2SO3,下列说法中不正确的是( )| A.升高温度,可以加快逆反应的速率 |
| B.增大氧气浓度可以加快正反应速率 |
| C.2体积的SO2和足量的O2反应可生成2体积的SO3 |
| D.正反应和逆反应速率相等时,该反应达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com