
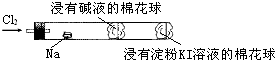
| A�� | ���Ż�ȼ�ղ�����ɫ���� | |
| B�� | ��Ӧ���ɵĴ����������Ȼ��ƾ��� | |
| C�� | ���в���һ�Ž���NaOH��Һ���������������չ�������������������Ⱦ���� | |
| D�� | ���Ҷ���������ɫ�仯���ж������Ƿ�Һ��ȫ���� |
���� A���ƵĻ���Ϊ��ɫ��
B������������Ӧ�����Ȼ��ư�ɫ���壻
C�������ж����ܹ����������Ʒ�Ӧ������������Һ���գ�
D����������ǿ�������ԣ��ܹ������⻯�����ɵ��ʵ⣬���������۱�����
��� �⣺A���ƵĻ���Ϊ��ɫ�����Dz�ɫ����A����
B������������Ӧ�����Ȼ��ư�ɫ���壬��������������̣���B��ȷ��
C�������ж����ܹ����������Ʒ�Ӧ������������Һ���գ���ֹ������Ⱦ����C��ȷ��
D����������ǿ�������ԣ��ܹ������⻯�����ɵ��ʵ⣬���������۱��������Թ��Ҷ���������ɫ�仯���ж������Ƿ�Һ��ȫ���գ���D��ȷ��
��ѡ��A��
���� ���⿼����Ԫ�ػ�����֪ʶ����Ϥ�Ƶġ����������ǽ���ؼ���ע����ɫ��ӦΪ���ʵ��������ʣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ԫ���⣬������Ԫ��ԭ�ӵ��������������ڸ�Ԫ�������������� | |
| B�� | ���������⣬�������ھ���18��Ԫ�� | |
| C�� | ����Ԫ�����зǽ���Ԫ�� | |
| D�� | �����Ԫ����ָ��A�������Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ԭ�� | a | b | c | d | e | f | g |
| M������� | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| A�� | a��c | B�� | a��f | C�� | d��g | D�� | e��g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KIO3��KI��������Һ�з�Ӧ��5I-+IO3-+3H2O=3I2+6OH- | |
| B�� | ��̼�������Һ�мӹ�������������Һ�����ȣ�NH4++OH-$\frac{\underline{\;��\;}}{\;}$NH3��+H2O | |
| C�� | ��NH4Al��SO4��2��Һ�е���Ba��OH��2��Һ��ǡ��ʹSO42-��ȫ������NH4++Al3++2SO42-+2Ba2++4OH-=Al��OH��3��+NH3•H2O+2BaSO4�� | |
| D�� | ��ϡ����ϴ���Թ��ڱڵ�������Ag+2H++NO3-=Ag++NO��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+ | B�� | K+ | C�� | Cl- | D�� | Ba2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
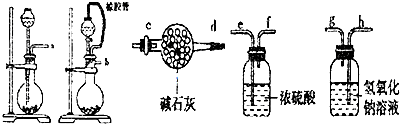
 ����ͼ��ʾ��װ�ã�
����ͼ��ʾ��װ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �ζ����� | �ζ�ǰ������mL�� | �ζ��������mL�� |
| 1 | 1.20 | 16.21 |
| 2 | 3.00 | 18.90 |
| 3 | 4.50 | 19.49 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | FeCl2��Һ��ͨ��Cl2��2 Fe2++Cl2=2 Fe3++2Cl- | |
| B�� | Al2O3��NaOH��Һ��Ӧ��Al2O3+2OH-=2 AlO2-+H2O | |
| C�� | FeCl3��Һ��ͭ��Fe3++Cu=Fe2++Cu2+ | |
| D�� | Cl2����ˮ��Cl2+H2O=2H++Cl-+ClO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԣ�HClO4��HBrO4��HIO4 | B�� | ���ԣ�NaOH��Mg��OH��2��Al��OH��3 | ||
| C�� | �е㣺HF��HBr��HCl | D�� | �ȶ��ԣ�PH3��H2S��HCl |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com