
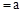 的CH3COOH稀溶液与pH
的CH3COOH稀溶液与pH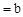 的NaOH稀溶液等体积混合,下列判断错误
的NaOH稀溶液等体积混合,下列判断错误A.若混合后pH ,则 ,则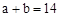 |
| B.反应过程中,CH3COOH的电离度增大 |
C.若混合后pH ,则c ,则c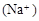 <c <c |
D.若混合后CH3COOH与NaOH恰好完全反应,则 |
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:不详 题型:单选题
| A.化石能源物质内部蕴涵着大量的能量 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C.物质的化学能可以在不同的条件下转化为热能、电能被人类利用 |
| D.吸热反应没有利用价值 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
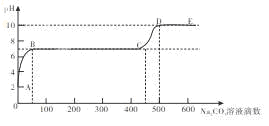
| A.开始时溶液pH=2是因为残留液中还有盐酸剩余 |
| B.AB段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加 |
| C.BC段发生的反应为:Ca2++CO32-= CaCO3↓ |
| D.滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4++ NH2-,25℃时,其离子积K=l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中不存在的关系式是(设温度保持不变,溶液体积为1L)
NH4++ NH2-,25℃时,其离子积K=l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中不存在的关系式是(设温度保持不变,溶液体积为1L)| A.c(Na+) = c(NH2-) | B.c (NH4+)=1×10-29mol/L |
| C.c(NH2-) > c (NH4+) | D.c(NH4+)?c(NH2-) = l.0×l0-30 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
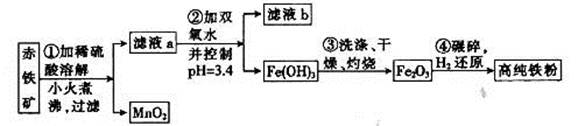
 Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
Fe2O3、3.6% FeO,还含有Al2O3、MnO2、CuO等。
 Cu(OH) 2+2H+的平衡常数K=_______。
Cu(OH) 2+2H+的平衡常数K=_______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大力提倡使用廉价化石燃料作为能源 |
| B.应更多地利用石油和煤生产基本化工原料 |
| C.化石燃料属于可再生能源,不影响可持续发展 |
| D.研发新型催化剂,提高石油和煤中各组分的燃烧热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加水稀释后,醋酸的电离程度增大,溶液的导电性增强 |
| B.c(H+)=c(CH3COO-)+c(OH-) |
| C.加入少量醋酸钠固体后,恢复至室温,溶液中c(CH3COO-)?c(H+)/c(CH3COOH)不变 |
| D.与等体积pH=11的NaOH溶液混合后,pH=7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L |
| B.混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
| C.c(OH-)-c(HY)=c(H+)=1×10-9 mol/L |
| D.c(Na+)=c(Y-)+c(HY)="0.3" mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com