
分析 (1)根据n=$\frac{m}{M}$计算D2O和H2O的物质的量,再利用分子的构成、原子的构成来计算中子数之比、电子数之比;
(2)等物质的量的D2O和H2O分别与足量的金属钠反应,则有2Na~H2↑,以此来计算氢气的质量关系;
(3)2CO2+2Na2O2=2Na2CO3+O2方程式中O2中的O元素全部来源于Na2O2,根据过氧化钠的质量计算.
解答 解:(1)设D2O和H2O的质量都是18g,
则n(H2O)=$\frac{18g}{18g/mol}$=1mol,
n(D2O)=$\frac{18g}{20g/mol}$=$\frac{9}{10}$mol,
则等质量的D2O和H2O所含的中子数之比为$\frac{9}{10}$mol×(1×2+8):1mol×8=9:8,
电子数之比为$\frac{9}{10}$mol×(1×2+8):1mol×(1×2+8)=9:10;
故答案为:9:8;9:10;
(2)等物质的量的D2O和H2O分别与足量的金属钠反应,
由2Na~2D2O~D2↑,2Na~2H2O~H2↑,
则放出的氢气的质量比为1mol×4g/mol:1mol×2g/mol=2:1,
故答案为:2:1;
(3)2CO2+2Na2O2=2Na2CO3+O2方程式中O2中的O元素全部来源于Na2O2,则m(O2)=$\frac{32×7.8g}{78×2}$=1.6g;
故答案为:1.6.
点评 本题考查物质的量的计算,明确质量、物质的量的关系,H、D的原子构成及Na与水的反应是学生解答本题的关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 回收废旧电池 | |
| B. | 加强控制燃放烟花爆竹法规 | |
| C. | 停止使用含铅汽油 | |
| D. | 将工厂烟囱加高,减少周围大气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
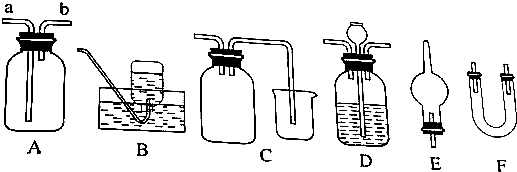
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LC5H12含有的分子数为0.5NA | |
| B. | 21g乙烯与丁烯的混合气体中含有3NA个C-H键 | |
| C. | 1L0.1mol/LNH4NO3溶液中含有0.2NA个N | |
| D. | 光照下,1molCl2与足量CH4完全反应,生成NA个HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
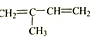 ⑤
⑤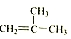
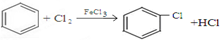 .
. .
. D.
D.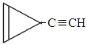 e.
e.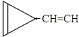 …
… 或
或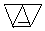 (只需答出一例的结构简式).
(只需答出一例的结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯和硝基苯均属于芳香烃 | |
| B. | 石油和天然气的主要成分都是碳氢化合物 | |
| C. | CH2=CHBr和CH3COCl 均属于卤代烃 | |
| D. | 分子内含有苯环和羟基的化合物都属于酚类 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com