
| A. | NH3 | B. | CO2 | C. | H2 | D. | Cl2 |
分析 极性分子中正负电荷的中心不重合,具有一定的极性,极性分子是由极性键构成的结构不对称的分子,非金属单质一般为非极性分子,以此解答该题.
解答 解:A.NH3中N原子形成3个δ键,有1个孤电子对,为sp3杂化,分子构型为三角锥形,空间结构不对称为极性分子,故A正确;
B.二氧化碳结构对称,正负电荷的中心重合,属于非极性分子,故B错误;
C.为非金属单质,只含有H-H键,为非极性分子,故C错误;
D.为非金属单质,只含有H-H键,为非极性分子,故D错误.
故选A.
点评 本题考查极性分子和非极性分子判断,为高频考点,侧重考查基本理论,难点是注意氨气和二氧化碳的极性判断,注意把握分子结构特点,为易错点,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH2Cl2的结构只有1种说明CH4是正四面体分子 | |
| B. | 苯不能使酸性高锰酸钾溶液,说明苯分子中不存在单键和双键交替的结构 | |
| C. | C2H4没有同分异构体,其与氯气加成的产物也没有同分异构体 | |
| D. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③①② | B. | ②①③ | C. | ③②① | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
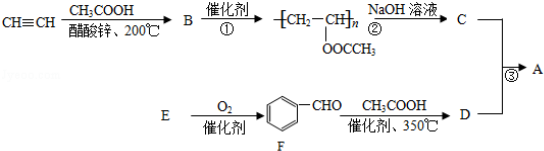

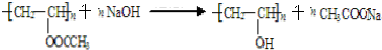 .
. .
. .
.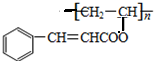 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应的发生无需任何条件 | |
| B. | 化学键断裂吸收能量,化学键形成放出能量 | |
| C. | 化学反应过程中的能量变化都是热量变化 | |
| D. | 只有化学反应过程中才有能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C4H10O的醇,能在铜催化和加热条件下被氧气氧化为醛的同分异构体共有4种 | |
| B. | 2-氯丁烷与NaOH乙醇的溶液共热的反应产物中一定不存在同分异构体 | |
| C. | 3-甲基-3-乙基戊烷的一氯代物有5种 | |
| D. | 分子式为C7H8O的有机物,能与氯化铁溶液发生显色反应的同分异构体共有3种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com