
【题目】常温下,将20.0g20.0%的NaCl溶液,跟10.0g35.0%的NaCl溶液混合,得到密度为1.17g/cm-3的混合溶液。计算:
⑴该混合溶液中溶质的质量分数;
⑵该混合溶液溶质的物质的量浓度;
⑶在500g水中需溶入多少摩尔NaCl,才能使其浓度恰好与上述混合溶液的浓度相等?
(计算结果保留小数点后一位)
科目:高中化学 来源: 题型:
【题目】已知A是一种装饰品的主要成分,根据如图转化关系,回答下列问题。
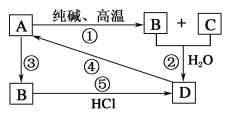
(1)A用途:_____________(任写一种),B是_____________,D是_____________。
(2)写出化学方程式:
①______________________________。
④______________________________。
(3)写出离子方程式:
②______________________________。
③______________________________。
⑤______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有Na+ 、Al3+ 、Cl – 、SO42-四种离子,已知Na+ 、Al3+ 、Cl –的个数比为3:2:1,则溶液中Al3+ 与SO42-物质的量之比为( )
A. 1:2 B. 1:4 C. 3:4 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期的A、B、C、D四种元素在周期表中均与元素X紧密相邻.已知元素X最高价氧化物的化学式为X2O5,B、D同主族且B元素的原子半径是同族元素中最小的,C的最高价氧化物对应的水化物是强酸.
(1)D元素基态原子的电子排布式为____________.
(2)A、C、X三种元素原子的第一电离能由大到小的顺序为_______________(用相应的元素符号作答).
(3)B、X、D氢化物的沸点由高到低的顺序为_______________(用相应的化学式作答).
(4)E元素是A元素所在周期中电负性最大的,试推测下列微粒的立体构型:
微粒 | EO2﹣ | EO3﹣ |
立体构型名称 |
(5)元素B的一种氢化物B2H4具有重要的用途.有关B2H4的说法正确的是____________.
A.B2H4分子间可形成氢键 B.B原子是sp3杂化
C.B2H4分子中含有5个σ键和1个π键 D.B2H4晶体变为液态时破坏共价键
(6)F元素基态原子M层上有5对成对电子,F形成的单质有δ、γ、α三种同素异形体,三种晶胞(如图所示)中F原子的配位数之比为____________,δ、γ、α三种晶胞的边长之比为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下22.4L HCl气体溶于水配成250mL溶液,此溶液中HCl的物质的量浓度为____________;将此10mL溶液加水稀释到100mL,稀释后溶液中HCl的物质的量浓度为___________;稀释后溶液中HCl的物质的量为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com