
����Ŀ����̼���⡢������Ԫ����ɵ�TMB��һ������ָ�Ƽ���ɫԭ�Լ�������Է�������Ϊ240��ij�о���ѧϰС���ͬѧ����������װ�òⶨTMB�ķ���ʽ��ʵ��ԭ�����������������н�4.80gTMB��Ʒ��������Ԫ��ת��ΪN2�������������ռ��ֱ�����ˮ������CO2 �� ���ͼ��ѡ���ʵ���װ�ã�����װ�ÿ����ظ�������ʵ�飮 
��1������a������Ϊ ��
��2��ʵ��װ���������ӵ�˳��Ϊ ��
��3��д��װ��C�з�Ӧ�Ļ�ѧ����ʽ�� ��
��4����ʵ�������Ҫ������Ҫ����β�������������� ��
��5��ʵ���Ƶ�װ��A����������14.08g��װ��B����������3.60g���ռ���0.56g����������ÿ�����վ�����ȫ�ģ�����TMB�ķ���ʽΪ ��
��6�����ʵ����֤CO2���������ԣ�
���𰸡�
��1��Բ����ƿ
��2��CBDBAA
��3��2H2O2 ![]() 2H2O+O2��
2H2O+O2��
��4������Ҫ��̼Ԫ�ر���ȼ����ȫ���ܱ�֤ʵ������ȷ�ԣ�û���ж�����ų�
��5��C16H20N2
��6������ĥ����þ����ȼ���������������̼�ļ���ƿ�У�þ������ȼ�գ�����ƿ���к�ɫ��������Ϊ̼���ʣ�˵��������̼����������
���������⣺C�й��������ڶ������̴�������������������Ũ�������������������TMB����Ϊ������̼��ˮ�͵������ü�ʯ�����ն�����̼��������Aװ������14.08g���������Ʒ��CԪ�ص����ʵ�����Bװ������3.60g���������Ʒ��HԪ�ص����ʵ������ٸ����ռ���0.56g�������������Ʒ��NԪ�ص����ʵ�������TMB������̼���⡢����ԭ�Ӹ����ȾͿ��������������Է�������֮�������Է������������ԭ�Ӹ����ȼ��������ʽ���Դ˽����⣬��1������ͼ�κ����ÿ�֪������aΪԲ����ƿ�����Դ��ǣ�Բ����ƿ����2����������������֪װ������Ϊ�Ʊ�������������������TMB������Ũ�����������ɵ�ˮ��������ʯ���������ɵĶ�����̼���塢������Ӽ�ʯ�ҷ�ֹ�����еĶ�����̼��ˮ��������װ��A���Ųⶨ�����װ������˳��Ϊ��CBDBAA��
���Դ��ǣ�CBDBAA����3�����������ڶ������������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2 ![]() 2H2O+O2����
2H2O+O2����
���Դ��ǣ�2H2O2 ![]() 2H2O+O2������4���������̼��ȫ���գ������ɵ����ǿ����ijɷ֣�û�б�Ҫ����β��������
2H2O+O2������4���������̼��ȫ���գ������ɵ����ǿ����ijɷ֣�û�б�Ҫ����β��������
���Դ��ǣ�����Ҫ����Ϊ̼Ԫ�ر���ȼ����ȫ���ܱ�֤ʵ������ȷ�ԣ�û���ж������ŷţ���5��ʵ���Ƶ�װ�ô��õ��Ⱥ�˳�����������ֱ�����3.60g��14.08g���ռ���0.56g��������m��H2O��=3.60g��m��CO2��=14.08g����
n��H2O��= ![]() =0.2mol��n��H��=0.4mol��
=0.2mol��n��H��=0.4mol��
n��CO2��= ![]() =0.32mol��n��C��=0.32mol��
=0.32mol��n��C��=0.32mol��
����n��N��= ![]() =0.04mol��
=0.04mol��
��n��C����n��H����n��N��=0.32mol��0.4mol��0.04mol=8��10��1��
TMB����Է�������Ϊ��2��120=240�������ʽΪ��C8nH10nNn �� ���У�12��8n+10n+14n=240�����n=2�����Է���ʽΪC16H20N2 ��
���Դ��ǣ�C16H20N2����6�����ʵ��ʹ������̼������Ӧ��̼Ԫ�ػ��ϼ۽��ͣ���������������ĥ����þ����ȼ���������������̼�ļ���ƿ�У�þ������ȼ�գ�����ƿ���к�ɫ��������Ϊ̼���ʣ�˵��������̼���������ԣ�
���Դ��ǣ�����ĥ����þ����ȼ���������������̼�ļ���ƿ�У�þ������ȼ�գ�����ƿ���к�ɫ��������Ϊ̼���ʣ�˵��������̼���������ԣ�


 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ��Ԥ��, 21������ľ�Ļ�����Ʒ������, ����ľ�ĵõ���ά��. ��������ά�ز��ܵõ���������(����)
A.����ֽ
B.������
C.ֽ��
D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��п/��Һ�����ܵ�ؽṹ��ͼ��ʾ������˵����ȷ���ǣ� �� 
A.�ŵ�ʱ��Na+���м��ҽ��븺����
B.���ʱ��Cl���������ҽ����м���
C.�ŵ�ʱ�������ĵ缫��ӦΪZn+4OH����2e��=Zn��OH��42��
D.���ʱ�������ĵ缫��ӦΪFe3++e��=Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������գ�
��1��I��20mL0.1mol/LBaCl2��Һ��Cl�������ʵ���Ũ��Ϊ �� Ba2+�����ʵ���Ϊ ��
��2��II����5.1gþ���Ͻ�ķ�ĩ��������������У��õ�5.6LH2����״���£��� �ٺϽ���þ�����ʵ��� ��
��д���úϽ���������NaOH��Һ�Ļ�ѧ����ʽ �� ͬʱ����H2���������״���£�Ϊ ��
��3��III����һ��������AlCl3��MgCl2�����Һ������һ����������������NaOH��Һ�����ɳ��������ʵ��������NaOH�����ʵ����Ĺ�ϵ��ͼ��ʾ���� 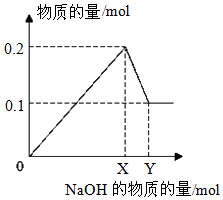
������Mg��OH��2��������
��X=��Y= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ȼ��飬Ҳ�м��ȣ�����������ɫ���壬�ܶ�Ϊ0.9159g/cm3 �� �۵�Ϊ��97.73�棬�е�Ϊ��24.2�棬18��ʱ��ˮ�е��ܽ��Ϊ280mL/mLˮ�������ѡ���ͪ���ܣ��������Ҵ�����ʵ�����������ͼװ������һ�ȼ��飺�Ʊ�װ�õķ�Һ©������ƿ�зֱ�ʢ�м״���Ũ���ᣮ 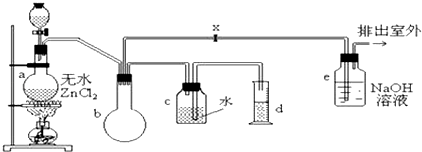
����д���пհף�
��1���Ʊ�һ�ȼ���Ļ�ѧ����ʽ �� �䷴Ӧ����������Ӧ��
��2��װ��b����������
��3����֪±�����ܷ�������ˮ�⣬ת��Ϊ����װ��e�п��ܷ����ķ�Ӧ����Ϊ�� ��
��4�������������CH3Cl�ķ����ǣ���e���ݳ��ڵ�ȼCH3Cl���壬���������ɫ��ȼ�ղ����к��Ȳ���ֻ��HCl������CH3Clȼ�յĻ�ѧ����ʽ����
��5��ʵ����ʵ�ʰ��״���Ũ����1��2��������֮�ȣ����з�Ӧ����������
��6��ijѧ���ڹرջ���x�����������ʵ��ʱ���֣��ռ���һ�������������������ĵļ״�Ũ����Ļ��Һ��������������¶ࣨװ�õ�������û�����⣩����ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ҹ������Ļ�ѧ�ң�1991����ȷ���In�����ԭ������Ϊ114.818�����������ԭ������ίԱ�����Ϊ�µı�ֵ���������ԭ�����������״β����ҹ��ⶨ�����ԭ������ֵ�������й��ڵ�˵���У�������ǣ�������
A.![]() Inԭ�Ӻ�����49������
Inԭ�Ӻ�����49������
B.![]() Inԭ�Ӻ�����49������
Inԭ�Ӻ�����49������
C.![]() In������Ϊ115
In������Ϊ115
D.![]() In��InԪ�ص�һ�ֺ���
In��InԪ�ص�һ�ֺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������������ȷ���ǣ� ��
A.���³�ѹ�£�11.2 L CO��CO2��������к��е�̼ԭ����ĿΪ0.5NA
B.��״���£�7.1 g��������������������Һ��Ӧת�Ƶĵ�����Ϊ0.2NA
C.���³�ѹ�£�4.6 g�Ҵ��к��еļ��Թ��ۼ���ĿΪ0.8NA
D.��1 L 1.0 molL��1̼������Һ�У���������������NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����ơ�����������Ʒ�Ӧ����װ�ã�ʵ��������ȸ���Ԥ�ȣ��������ڳ�Բ��ʱ��ֹͣ���ȣ�ͨ�����������ɼ����Ż�ȼ �գ��������������̣���������������ǣ�������
A.���Ż�ȼ�ղ�����ɫ����Ͱ���
B.�������Ȼ�������ɢ�ڿ������γ�
C.�����в���һ�Ž���NaOH��Һ��������Ϊ�����չ������������Է���Ⱦ����
D.���ݹ��Ҷ�������ɫ�ı仯��������ж������Ƿ�Һ��ȫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ�ƿ��ǩ�ϵIJ������ݣ����ø�Ũ��������500mLŨ��Ϊ1molL��1��ϡ���ᣮ�ɹ�ѡ�õ������У� 
�ٲ����� ���ձ� ��������ƽ ����Ͳ ��ҩ�� ��ͷ�ι� ��500mL����ƿ ��ϸ���Լ�ƿ
��ش��������⣺
��1������500mLŨ��Ϊ1molL��1��ϡ���ᣬ������Ͳ��ȡ ����Ũ�������ΪmL��
��2������ʱ��һ��ɷ�Ϊ���¼������裺����ȡ �ڼ��� ��ϡ�� ��ҡ�� ��ת�� ��ϴ�� �߶��� ����ȴ������ȷ�IJ���˳��Ϊ �� ����������������ѡȡ
����Ҫ�������� ��
��3��ʵ���������õ���������������ֱ� �� ��
��4�������ƹ����У����в���������������ҺŨ��ƫ����������ţ�
A.ϴ����ȡŨ�������Ͳ������ϴ��Һת�Ƶ�����ƿ��
B.δ��ϡ�ͺ��������Һ��ȴ�����¾�ת�Ƶ�����ƿ��
C.ת��ǰ������ƿ�к�����������ˮ
D.δϴ��ϡ��Ũ����ʱ�ù����ձ��Ͳ�����
E.����ʱ�����ӿ̶���
F.����ʱ��ˮ�����˿̶��ߣ������ý�ͷ�ι���ȥ�����ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com