
把一定质量的镁、铝混合物投入到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。

(1)金属铝的质量为____________。
(2)a的取值范围是________________。
(3)盐酸的体积是________mL。
(4)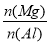 的最大值是____________。
的最大值是____________。
(5)80~90 mL对应反应的离子方程式________________。
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:选择题
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
A.2Na + 2H2O ==2NaOH + H2↑ B.CH4 + 2O2点燃 CO2 + 2H2O
C.2KClO3加热2KCl + 3O2↑ D.CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省宝安第一外国语学校高一上期中考试化学试卷(解析版) 题型:选择题
某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不与酸反应),跟大量废盐酸接触形成污水,产生公害。若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是( )
A.Fe2+、Cu2+ B.Cu2+、H+ C.Zn2+、Fe2+ D.Zn2+、H+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列物质在水溶液中的电离方程式错误的是( )
A.Na2CO3= 2Na+ + CO32- B.NaHSO4= Na+ + H+ + SO42-
C.KOH= K+ + O2- + H+ D.H2SO4= 2H+ + SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:选择题
将2.32 g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )

A.OA段发生反应的离子方程式为:H++OH-===H2O CO+H+===HCO
B.当加入35 mL盐酸时,产生CO2的体积为224 mL(标准状况)
C.A点溶液中的溶质为NaCl、NaHCO3
D.混合物中NaOH的质量0.60 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期12月月考化学试卷(解析版) 题型:选择题
在两个烧杯中分别盛有100 mL 3.0 mol·L-1的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2∶5,则加入的铝粉的质量为( )
A.2.7 g B.5.4 g C.6.75 g D.8.1 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期第三次月考化学试卷(解析版) 题型:填空题
重水(D2O)的离子积Kw=1.6×10 -15 mo12·L-2.,可以用pH一样的定义来规定 pD=—lg[D+],试求该温度下:(已知lg5=0.6990 ;lg3=0.4771 ;lg2=0.3010;计算时选取合适的数据)
①重水的pD= ;
②含0.01molNaOD的D2O溶液1L,其pD= ;
③溶解0.01molDCl的D2O溶液1L,其pD= ;
④在100mL0.25mol.L-1的DCl重水溶液中,加入50mL0.2 mo1·L-1的NaOD的重水溶液,其pD= ;
查看答案和解析>>
科目:高中化学 来源:2016届广东省东莞市六校高三上学期联考理综化学试卷(解析版) 题型:选择题
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
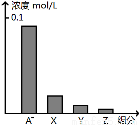
A.HA为强酸 B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+ D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省沈阳市四校协作体高三上学期期中联考化学试卷(解析版) 题型:填空题
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断试样的pH约为 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:
2H2(g)+O2(g)=2H2O(g)ΔH =-483.6 kJ·mol-1
2C(s)+O2(g)=2CO(g)ΔH =-221.0 kJ·mol-1
则C(s)+ H2O(g)=CO(g)+ H2(g)ΔH=____ ___ kJ·mol-1。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是 。
A.Ca(OH)2 B.Na2CO3 C.CaCl2 D.NaHSO3
(3)汽车尾气中有NOx和CO的生成:
①已知气缸中生成NO的反应为:N2 (g)+O2(g) 2NO(g)△H
2NO(g)△H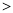 0
0
ⅰ.若1L空气含0.8molN2和0. 2molO2,1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K= 。
ⅱ.恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是
A混合气体的密度不再变化
B混合气体的平均分子量不在变化
C N2 、O2、NO的物质的量之比为1:1:2
D氧气的百分含量不在变化
ⅲ.若升高温度,则平衡___________(填“正向”或“逆向”或“不”下同)移动,逆反应速率 (填“变大 ”或“变小”或“不变”)。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO,2CO(g)=2C(s)+O2(g)。已知该反应的△H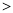 0,则该设想能否实现 (填“能”或“不能”)?
0,则该设想能否实现 (填“能”或“不能”)?
(4)综上所述,你对该市下一步的环境建设提出的建议是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com