
【题目】KO2的晶体结构和NaCl相似,KO2可以看作是Na+的位置用K+代替,Cl-的位置用O2-代替,则关于KO2晶体结构的描述正确的是( )
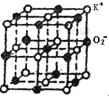
A.如图一个超氧化钾小晶胞中含有4个KO2
B.和K+距离相同且最近的O2-构成的多面体是正六面体
C.和K+距离相同且最近的K+有8个
D.和K+距离相同且最近的O2-共有8个
【答案】A
【解析】
根据题意及观察晶体结构可知,一个超氧化钾小晶胞是一个立方体,每个离子周围有6个离它最近的异号离子;K+占据晶胞的8个顶点和6个面心,每个晶胞占有K+数为:8×![]() +6×
+6×![]() =4;O2-占据晶胞的12条棱心和体心,每个晶胞占有O2-数为:12×
=4;O2-占据晶胞的12条棱心和体心,每个晶胞占有O2-数为:12×![]() +1=4。可在此基础上对各选项作出判断。
+1=4。可在此基础上对各选项作出判断。
A. 根据分析,图中一个超氧化钾小晶胞中含有4个K+和4个O2-,所以一个超氧化钾小晶胞中含有4个KO2,A选项正确;
B. 和K+距离相同且最近的O2-有6个:上、下、左、右、前、后各1个,构成的多面体是正八面体,B选项错误;
C. 根据晶胞的含义,观察晶胞结构可知,K+距离相同且最近的K+有12个,C选项错误;
D. 由B选项可知,和K+距离相同且最近的O2-共有6个,D选项错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】五氧化二钒用作冶金添加剂,占五氧化二钒总消耗量的 80%以上,其次是用作有机化工的催化剂。为了增加V2O5 的利用率,我们从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2 和Fe2O3 等) 中回收 V2O5 的一种生产工艺流程示意图:
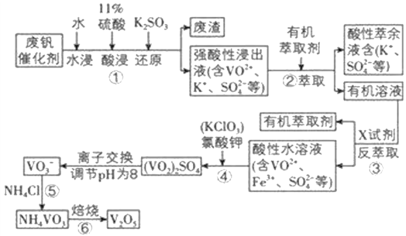
部分含钒物质在水中的溶解性如表所示,回答下列问题:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(1)①中废渣的主要成分是 __________________________;①中V2O5 发生反应的离子方程式为 ___________________________ 。
(2)②、③中的变化过程可简化为(下式中的R 表示 VO2+或 Fe3+,HA 表示有机萃取剂的主要成分)R2(SO4)n(水层)+2nHA(有机层) 2RA(有机层)+ nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是 ______________________;实验室进行萃取操作使用的玻璃仪器为 ______________________。
(3)实验室用的原料中V2O5 占 6%(原料中的所有钒已换算成 V2O5)。取 100 g 该废钒催化剂按工业生产的步骤进行实验,当加入 100 mL 0.1 molL -1 的KClO3 溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是 __________________[M(V2O5)=182 gmol -1]。
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液 pH 之间的关系如表所示:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 |
钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 |
试判断在实际生产时,⑤中加入 NH4Cl 调节溶液的最佳 pH为____________;若钒沉淀率为 93.1%时不产生 Fe(OH)3 沉淀,则此时溶液中 c(Fe3+)≤____________ (已知:25℃时Ksp[Fe(OH)3]=2.6×10 -39)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是第四周期第ⅥA族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ΔH1=akJ·mol-1
2Se(s)+2H2O(l) ΔH1=akJ·mol-1
②2H2(g)+O2(g)![]() 2H2O(l) ΔH2=bkJ·mol-1
2H2O(l) ΔH2=bkJ·mol-1
反应H2(g)+Se(s)![]() H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
H2Se(g)的ΔH3=__kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1molSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①下列情况可判断反应达到平衡状态的是__(填字母代号)。
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为H2Se液体,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释:_。
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图1、图2所示:
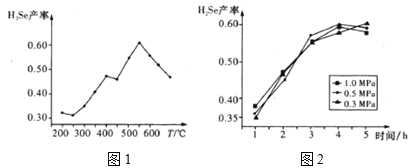
则制备H2Se的最佳温度和压强为__。
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈__(填“酸性”或“碱性”),请通过计算数据说明__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵(NH4Fe(SO4)2·xH2O)是一种重要铁盐,为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁氨,具体流程如下:

(1)步骤②需要加热的目的是_______________
(2)步骤②温度保持80-95℃,采用的合适加热方式是_____________________
(3)步骤③加入5%H2O2的目的是将Fe2+全部氧化为Fe3+,不引入杂质,请写出反应的离子方程式__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅晶体是立体的网状结构,其结构如图所示.关于二氧化硅晶体的下列说法不正确的是( )
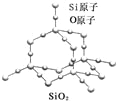
A. 晶体中Si、O原子个数比为1:2
B. 晶体中Si、O原子最外层都满足8电子结构
C. 晶体中一个硅原子含有Si﹣O键数目为4
D. 晶体中最小环上的原子数为6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钙[Ca(IO3)2]是重要的食品添加剂。实验室制取Ca(IO3)2·H2O的实验流程:
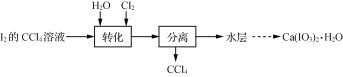
已知:碘酸是易溶于水的强酸,不溶于有机溶剂。
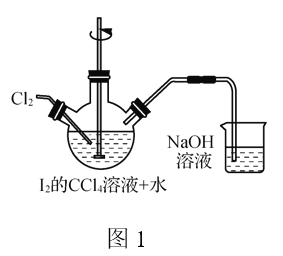
(1) 转化步骤是为了制得碘酸,该过程在图1所示的装置中进行,当观察到反应液中紫红色接近褪去时,停止通入氯气。
①转化时发生反应的离子方程式为_____________________________________。
②转化过程中CCl4的作用是_______________________________________。
③为增大转化过程的反应速率,可采取的措施是_______________________。
(2)将CCl4与水层分离的玻璃仪器有烧杯、________。除去HIO3水溶液中少量I2单质的实验操作为______________________________,直至用淀粉溶液检验不出碘单质的存在。
(3)已知:①Ca(IO3)2·6H2O是一种难溶于水的白色固体,在碱性条件下不稳定。
②Ca(IO3)2·6H2O加热升温过程中固体的质量变化如图2所示。
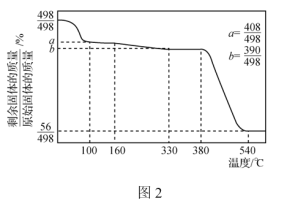
设计以除碘后的水层为原料,制取Ca(IO3)2·H2O的实验方案:向水层中__________。[实验中必须使用的试剂:Ca(OH)2粉末、AgNO3溶液]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳钢广泛应用在石油化工设备管道等领域,随着深层石油天然气的开采,石油和天然气中含有的CO2及水引起的腐蚀问题(俗称二氧化碳腐蚀)引起了广泛关注。深井中二氧化碳腐蚀的主要过程如下所示:
负极:![]() (主要)
(主要)
正极:![]() (主要)
(主要)
下列说法不正确的是
A.钢铁在CO2水溶液中的腐蚀总反应可表示为![]()
B.深井中二氧化碳对碳钢的腐蚀主要为化学腐蚀
C.碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含量高腐蚀速率会加快
D.腐蚀过程表明含有CO2的溶液其腐蚀性比相同pH值的HCl溶液腐蚀性更强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列原子构成的单质中既能与稀硫酸反应,又能与烧碱溶液反应,且都产生H2的是
A. 核内无中子的原子
B. 外围电子构型为3s23p4的原子
C. 核外电子排布图为![]()
![]() 的基态原子
的基态原子
D. 处于激发态时其原子的电子排布式可能为1s22s22p63s13p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物柴油是指由动植物油脂(脂肪酸甘油三酯)与醇(甲醇或乙醇)经酯交换反应得到的脂肪酸单烷基酯,可以替代普通柴油使用的清洁的可再生能源。某同学利用菜籽油与甲醇制备生物柴油,其原理及实验步骤:
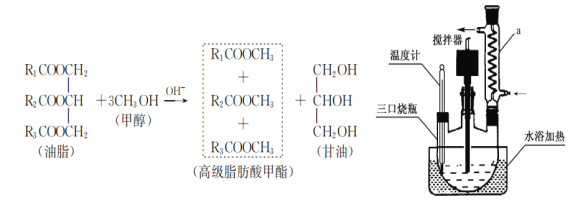
①称取4.6g CH3OH和0.2g NaOH依次放入锥形瓶中,充分震荡得NaOH溶液甲醇溶液;
②将20g 菜籽油、20g正己烷(作溶剂)、步骤1配得的NaOH甲醇溶液一次加入到三口烧瓶中;
③安装装置(如图)恒温水浴加热,使温度保持在60~65℃左右,搅拌速度400r/min,回流1.5h~2h;
④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
(1)仪器a的名称是_________________ 。
(2)试验中取用的甲醇与油脂的物质的量之比约为6:1,甲醇过量的主要目的是________________;NaOH的用量不宜过多,其原因是____________________________。
(3)步骤4的液体分为两层,上层为生物柴油、正己烷和甲醇。下层主要为甘油、分离出下层液体的方法是_______________________________________ ;上层液体需用温水洗涤,能说明已洗涤干净的依据是____________________________________。
(4)碘值是指每100g油品所能吸收碘(I2)的质量。测定产品碘值得步骤如下:
I.准确称取m g 油品,注入碘量瓶中,向碘量瓶中加入20 mL氯仿溶解后,加入25.00mL韦氏碘液,(IBr溶液及催化剂,发生反应:![]() ),立即加塞,摇匀后,将碘量瓶放于黑暗处。
),立即加塞,摇匀后,将碘量瓶放于黑暗处。
II.30min 后立即加入20 mL 15%的碘化钾溶液和100 mL水,发生反应的化学方程式为 __________________________________________ ,不断震荡,用c mol·L-1 的Na2S2O3溶液滴定至溶液呈浅黄色时,加入1mL 淀粉指示剂,继续滴定(I2 + 2Na2S2O3=2NaI+Na2S4O6),至终点是消耗V1 mL Na2S2O3溶液。滴定终点的现象是 ______________________________________________ 。
III.另做空白对照试验,除不加油品外,其余操作同上,至终点时消耗V2 mL Na2S2O3溶液。则测得的油品的碘值为__________________ g/100g (列出计算表达式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com