
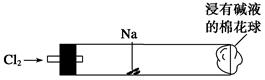
| A����Ӧ���ɵĴ����������Ȼ��ƾ��� |
| B�����Ż�ȼ�տ���CO2��� |
| C��������β������NaOH��Һ���������������չ�������������������Ⱦ���� |
| D�����������Ҳ����ص�һ�ε��۵⻯����Һ���ɾ�����ɫ�仯�ж������Ƿ�Һ��ȫ���� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʯ��ˮ | B��NaOH��Һ | C������ | D��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A�����Ż����ȼ�ղ�����ɫ�Ļ��� |
| B����Ӧ�����Ĵ����������Ȼ��ƹ��� |
| C������ٵ����������չ���������ֹ������Ⱦ |
| D������ڱ���ɫ��֤������δ����Һ��ȫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����a mol AlCl3����Һ�ͺ�1.5a mol NaOH����Һ���������κͷ��Σ����ɵ�Al(OH) 3��������� |
| B����a mol Na2CO3����Һ�ͺ�1.5a mol HCl��ϡ����,�������κͷ���,���ɵ�CO2��� |
| C����������NaHCO3��Na2CO3�ֱ����������ᷴӦ����ͬ��ͬѹ��,���ɵ�CO2�����ͬ |
| D���������������ɲ�ͬ�����ƺϽ�ֱ�Ͷ�뵽���������У����ų���H2Խ�࣬��������������ԽС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(OH��) > c(HCO3��) |
| B��c(HCO3��) > c(CO32��) |
| C��c(Na+) = 2c(CO32��) + 2c(HCO3��) + 2c(H2CO3) |
| D��c(Na+)+c(H+) = c(HCO3��)+2c(CO32��)+c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2O2��Na2O | B��Na2O |
| C��Na2O2 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
| ʱ�䣯s | 0 | 5 | 10 | 15 |
| ������g | 215.2 | 211.4 | 208.6 | 208.6 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com