
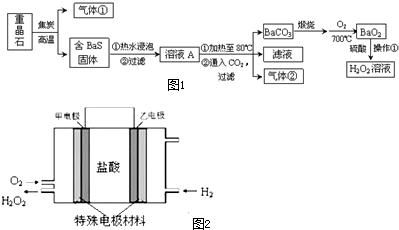
分析 重晶石是BaSO4,由BaSO4和单质碳高温生成气体:BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO↑.碳、一氧化碳高温燃烧生成气体CO2,BaS溶于H2O遇二氧化碳反应:BaS+H2O+CO2=BaCO3↓+H2S,硫化氢燃烧生成二氧化硫,含BaS的固体热水浸泡,2BaS+2H2O?Ba(OH)2+Ba(HS)2,过滤得到溶液A,通二氧化碳:Ba(HS)2+CO2+H2O=BaCO3↓+2H2S,Ba(OH)2+CO2=BaCO3↓+H2O,气体②为硫化氢,BaCO3$\frac{\underline{\;高温\;}}{\;}$BaO+CO2↑,2BaO+O2$\frac{\underline{\;300℃\;}}{\;}$2BaO2,BaO2+H2SO4=BaSO4↓+H2O2.
(1)生产过程中会产生大量废气(主要成分为CO2、CO及少量SO2和硫蒸气等);
(2)在溶液中,硫离子水解导致溶液显示碱性;
(3)根据盖斯定律书写CO2 和Ba(HS)2反应的热化学反应方程式,根据影响化学平衡因素分析需将溶液A加热的原因;
(4)BaS不能存在于水中,BaS溶于水后,S元素主要以HS-的形式存在,故溶液A中存在大量Ba2+和HS-,和H2O、CO2反应生成CaCO3、H2S气体,即气体B的主要成分为H2S气体,H2S气体可用来制造H2SO4;
(5)根据溶解平衡常数计算;
(6)电极方程式的书写:先写出反应物、产物、电子,根据电荷守恒写出H+,原子守恒配平.
解答 解:(1)由BaSO4和单质碳高温生成气体:BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO↑.碳、一氧化碳高温燃烧生成气体CO2,BaS溶于H2O遇二氧化碳反应:BaS+H2O+CO2=BaCO3↓+H2S,硫化氢燃烧生成二氧化硫,所以图1中的气体①可能①CO②CO2③SO2都有,
故答案为:D;
(2)在硫化钡中,硫离子水解而使得硫化钡显碱性,有碱Ba(OH)2生成,硫离子水解生成HS-,即2BaS+2H2O?Ba(OH)2+Ba(HS)2,
故答案为:2BaS+2H2O?Ba(OH)2+Ba(HS)2;
(3)Ba(OH)2(aq)+CO2(g)=BaCO3(s)+H2O(l)△H=-162kJ•mol-1①
2H2S(g)+Ba(OH)2(aq)=Ba(HS)2(aq)+2H2O(l)△H=-191kJ•mol-1②根据盖斯定律将①-②得:Ba(HS)2(aq)+CO2(g)+H2O(l)=BaCO3(s)+2 H2S(g)△H=+29kJ•mol-1,该反应为吸热反应,加热可使平衡向正反应方向移动,提高BaCO3产率,
故答案为:Ba(HS)2(aq)+CO2(g)+H2O(l)=BaCO3(s)+2 H2S(g)△H=+29kJ•mol-1;上述反应为吸热反应,加热可使平衡向正反应方向移动,提高BaCO3产率;
(4)BaS不能存在于水中,BaS溶于水后,S元素主要以HS-的形式存在,故溶液A中存在大量Ba2+和HS-,和H2O、CO2反应生成CaCO3、H2S气体,即气体B的主要成分为H2S气体,H2S气体和与氧气反应生成二氧化硫、二氧化硫和氧气反应生成三氧化硫,三氧化硫和水反应生成硫酸,所以硫化氢可用来制造H2SO4,
故答案为:H2SO4;
(5)有BaSO4沉淀的溶液中:Ksp(BaSO4)=cC(Ba2+)•C(SO42-)=1×10-10,若测得SO42-的浓度为1×10-4mol•L-1,则:cC(Ba2+)=$\frac{{K}_{SP}(BaS{O}_{4})}{C(S{{O}_{4}}^{2-})}$=$\frac{1×1{0}^{-10}}{1×1{0}^{-4}}$=1×10-6mol•L-1,即该溶液中Ba2+的浓度为1×10-6mol•L-1,要生成BaCO3沉淀,需要满足cC(Ba2+)•C(CO32-)≥Ksp(BaCO3)=2.5×10-9
C(CO32-)≥$\frac{{K}_{SP}(BaC{O}_{3})}{C(B{a}^{2+})}$=$\frac{2.5×1{0}^{-9}}{1×1{0}^{-6}}$=2.5×10-3mol•L-1;
故答案为:2.5×10-3mol•L-1;
(6)据图2所示甲电极上消耗O2,生成H2O2,1molO2生成1molH2O2时失去2mol电子,电解质溶液为盐酸,酸性条件下,离子反应方程式为:2H++O2+2e-=H2O2;
故答案为:2H++O2+2e-=H2O2.
点评 本题以重晶石(BaSO4)为原料制备过氧化氢为载体,考查物质推断、热化学方程式的书写、水解化学方程式书写、沉淀转化的有关知识以及电极方程式的书写等,是对所学知识的综合运用与能力的考查,根据已有知识结合工艺流程推断物质及发生反应是解题关键,题目难度中等.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 酸的水溶液呈酸性;则有酸性的水溶液也一定是酸的水溶液 | |
| B. | Fe3O4可写成FeO?Fe2O3;Pb3O4也可写成PbO?Pb2O3 | |
| C. | 可电解熔融MgCl2来制取金属镁;也能电解熔融HCl来制取氢气 | |
| D. | 第2周期元素氢化物稳定性顺序是HF>H2O>NH3;则第3周期元素氢化物稳定性顺序是HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、④
、④ 、⑤
、⑤ 、⑥
、⑥ .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
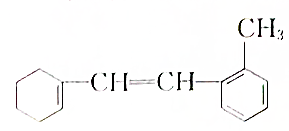 [典型例题√某有机物的结构简式如图:
[典型例题√某有机物的结构简式如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式: | B. | 石炭酸的结构简式:C6H5OH | ||
| C. | 乙醛的分子式:C2H4O | D. | 酚醛树脂的结构简式为 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com