
A.X2Y B.XY
科目:高中化学 来源: 题型:
 (2011?崇川区三模)已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子.
(2011?崇川区三模)已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子. ]-
]- ]-
]-| 1 |
| 8 |
| 270 | ||
|
| 270 | ||
|
查看答案和解析>>
科目:高中化学 来源:必修二训练化学苏教版 苏教版 题型:022
历史上,为了寻求各种元素及其化合物间的内在联系和规律性,许多人进行了各种尝试.1869年________国化学家________在前人探索的基础上发现了元素周期律,从而加速了化学科学发展的进程.元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表给出了1-18号元素在周期表中的位置.
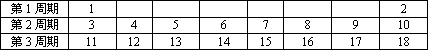
(1)原子序数为17的元素名称是________,在化学反应中,该元素的原子容易________(填“得”或“失”)电子;原子序数为13的元素属于________(填“金属”或“非金属”)元素.
(2)对上表进行研究,可以发现如下规律:
①原子序数与元素原子的核电荷数在数值上相等;
②________;
③________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省唐山市高三4月第二次模拟理综化学试卷(解析版) 题型:推断题
X、Y、Z、W、R为前四周期原子序数依次增大的五种元素,X、Y、Z、W为同一周期相邻元素,Z元素原子核外电子的运动状态共有8种;R元素与比它核电荷数大的另外两种元素位于第四周期同一族。
(1)X的一种核素用于鉴定文物年代,该核素的符号为____。
(2)X、Y、Z、W四种元素第一电离能由大到小的顺序为____(用元素符号表示)。
(3)用氢键表示式写出W的气态氢化物水溶液中不同种分子间存在的氢键____。
(4)Y的一种氢化物分子中共有18个电子,该分子中存在的共价键类型有____(填选项字母)。
A.非极性键;B.极性键;C. 键;D.
键;D. 键;E.p—p
键;E.p—p 键;F.
键;F. 键;G.
键;G. 键;H.
键;H.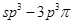 键
键
(5)R的基态原子的价层电子排布式为____,R元素位于周期表的____区。
(6)R单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图所示:

图A中原子堆积方式为 ,A、B中R原子的配位数之比为____。A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
第1周期 | 1 |
|
|
|
|
|
| 2 |
第2周期 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
第3周期 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
(1)原子序数为 17的元素名称是_____________,在化学反应中,该元素的原子容易_____________(填“得”或“失”)电子;原子序数为 13的元素属于_____________(填“金属”或“非金属”)元素。
(2)对上表进行研究,可以发现如下规律:
①原子序数与元素原子的核电荷数在数值上相等;
②_________________________________________________________________;
③__________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com