
��15�֣�ij�о�С���û�ͭ����Ҫ�ɷ���CuFeS2������SΪ-2�ۣ�Ϊ��Ҫԭ����ͭ�����ܷ�ӦΪ��2CuFeS2+2SiO2+5O2��2Cu+2FeSiO3+4SO2����ʵ�ϸ÷�Ӧ�ǰ��������̷ֲ����еģ�
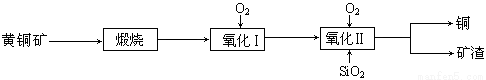
��1��������ķ�Ӧ��Ҫ���������ɵ�����������һ������Ϊ��������������������跴Ӧ���ɿ�������������Ҫ�ɷ��� ���ѧʽ����
��2���ݱ�������һ��ϸ�������������¿��Խ���ͭ�������������Σ���Ӧ����������Һ�з����ġ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3���ҹ�ѧ���о����֣��Ծ�CuFeS2��Ϊԭ���ڷ���¯����O2����������Ӧ����������ȴ���ܽ⡢�������ᾧ���õ�CuSO4��5H2O�������ɱ��ܹ��������ࡣ�й�ʵ�������±���
����¯�¶�/�� | 560 | 580 | 600 | 620 | 640 | 660 |
ˮ����Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
������Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 |
��CuFeS2��O2��Ӧ�Ļ�ѧ����ʽΪ ��
��ʵ�����������з���¯�¶�Ϊ600��620 �档������¶ȵķ����� ��
�۵��¶ȸ���600��620 ��ʱ����������ˮ����ͭ�½���ԭ���� ��
����������ȴ��ij�����ʵ�����������Ҫ�� ����֪����Һ�У�Cu2+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ4.7��6.7��Fe3+��ʼ�����ͳ�����ȫ��pH�ֱ�Ϊ1.1��3.2������Ƶõ�����ͭ��Һ�к���������Fe3+����д����ȥ��Һ��Fe3+��ʵ��������裺 ��
��15��
��1��FeSiO3��2�֣�
��2��4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O��2�֣�
4CuSO4+2Fe2(SO4)3+2H2O��2�֣�
��3����4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2��2�֣�
�ڿ��Ƽ���CuFeS2���ٶȣ���CuFeS2��O2��Ӧ���ȣ���2�֣�
��CuSO4���ȷֽ⣨2�֣�
�ܹ��ˣ�2�֣� ����CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ��ã�������ϡ�����ữ��3�֣�
��������
�����������1������2CuFeS2+2SiO2+5O2��2Cu+2FeSiO3+4SO2���ɵÿ���ΪFeSiO3��
��2���������֪��CuFeS2��������Һ����������һ��ϸ�������������ɵ�������������ͭ������������ѧ����ʽΪ4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O��
4CuSO4+2Fe2(SO4)3+2H2O��
��3���پ�CuFeS2��Ϊԭ���ڷ���¯����O2����������Ӧ�����յ�CuSO4��5H2O��˵����Ԫ�صĴ�����ʽ������������ˮ�ܽ�ɹ��˳�ȥ������CuFeS2��O2��Ӧ�Ļ�ѧ����ʽΪ4CuFeS2+15O2��4CuSO4+2Fe2O3+4SO2
����ΪCuFeS2��O2��Ӧ���ȣ����������������п��Ƽ���CuFeS2���ٶȣ������¶ȣ�
��ˮ����ͭ������ΪCuSO4?5H2O��������ͭ������ΪCuO���¶Ƚϸ�ʱ��CuSO4?5H2O�ɷֽ�����CuO������600������ʱˮ����ͭ�����ﺬ�����٣�
���������г�����ͭ�����������������������ˮ��������ȴ��ij�����ʵ�����������Ҫ�ǹ��ˣ���ȥ�����Ӷ�����ȥͭ���ӣ�������Һ��pHֵ��3.2��4.7֮�䣬ʹ��������ȫ��������ͭ���Ӳ����������Ծ�������Ǽ���CuO[��Cu(OH)2��CuCO3]��ĩ����ֽ��裬������Һ��pHԼΪ3.2��������У����ˣ��ã�������ϡ�����ữ��
���㣺���������Ʊ�������ͼ�ķ�������ѧ����ʽ����д



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���г��ӷ�����ȷ����
A����������ȥ�����л��е�������ϩ
B���ý����Ƴ�ȥ�Ҵ��л��е�����ˮ
C�������Ը��������Һ��ȥ�����л��е�������ϩ
D���ñ���̼��������Һ��ȥ������̼�л��е������Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�߶���ѧ�ڽβ���5�� ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ��װ�ý��е���Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
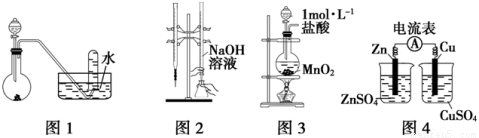
A����ͼ1��ʾװ�ý���ϡ������ͭ�ķ�Ӧ��ȡ���ռ�NO
B����ͼ2��ʾװ�ý�������֪Ũ�ȵ�����������Һ�ⶨ����Ũ�ȵ�ʵ��
C����ͼ3��ʾװ����ȡ����Cl2
D����ͼ4��ʾװ�ü�������ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
Q��W��X��Y��Z��ԭ��������������Ķ�����Ԫ�أ�X����ɫ��Ӧ�ʻ�ɫ��QԪ�ص�ԭ�����������������ڲ��������2����W��Z������������ͬ��Z�ĺ˵������W��2����Ԫ��Y�ĺϽ����ճ�������ʹ����㷺�Ľ�������֮һ������˵����ȷ����
A��ԭ�Ӱ뾶�Ĵ�С˳��rX>rY> rW >rQ
B��X��Y������������ˮ����֮�䲻�ܷ�����Ӧ
C��Ԫ��Q��Z���γ�QZ2�͵Ĺ��ۻ�����
D��ZԪ�ص��⻯���ȶ��Դ���WԪ�ص��⻯���ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и���������ָ����Һ��һ���ܴ����������
A��1.0 mol/L��NaHSO4��Һ��K+��Fe2+��NO3����Cl��
B��l.0 mol��L��1 NaClO��Һ��Fe2+��K+��Iһ��Cl��
C�������Ի�ɫ����Һ�� Na+��CO32����NO3����SO32��
D����c(H+)��c(OH��) = 1��1013����Һ��NH4+��Ca2+��C1����K+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
25 ��ʱ��2a mol��L��1������ˮ��Һ�У���NaOH��Һ������pH��������Һ����ı仯�����õ�c(HClO)��c(ClO��)����ҺpH�ı仯��ϵ��ͼ��ʾ������˵����ȷ����
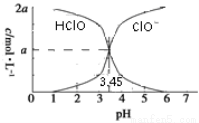
A����pH��2ʱ����Һ��c(ClO��)��c(Na��)
B����c(ClO��)��c(HClO)ʱ����Һһ���ʼ���
C����pH��3.45ʱ������NaOH��Һǡ����HClO��ȫ��Ӧ
D����pH��5ʱ����Һ�У�c(HClO)��c(Na��)��c(H��)��c(OH��)��2a mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ������˵����ȷ����
A�����³�ѹ�£�32 g �״��к��е�C��H������ĿΪ4NA
B����״���£�11.2 L ��ȩ�к��еĵ�����ĿΪ8NA
C��0.1 mol N2��0.3 mol H2��һ�������³�ַ�Ӧ�����ɵİ�������ĿΪ0.2NA
D��1 L 0.01 mol��L��1 KAl(SO4)2��Һ�У����е���������ĿΪ0.02NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���������ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��άA����һ��Ƥ������ҩ������ԭ��X�����ಽ��Ӧ�ϳɣ�
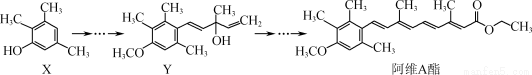
����������ȷ����(����)
A�� �л���X��Y��Ϊͬϵ��
B�� �л���Y�밢άA��������NaOH��Һ��Ӧ
C�� һ��������1 mol��άA������4 mol H2�����ӳɷ�Ӧ
D�� X����6�ֻ�ѧ������ͬ����ԭ�ӣ�Y����1������̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�⽭�и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���д�С��ϵ�Ƚ���ȷ����
A�����Ӱ뾶��F��<Na+<Mg2+B���縺�ԣ�C<O<N
C���⻯��ķе㣺NH3<PH3<AsH3D�����ԣ� NaOH)>Mg(OH)2> Al(OH)3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com